Questão 12
(EsPCEx - 2016)
Compostos contendo enxofre estão presentes, em certo grau, em atmosferas naturais não poluídas, cuja origem pode ser: decomposição de matéria orgânica por bactérias, incêndio de florestas, gases vulcânicos etc. No entanto, em ambientes urbanos e industriais, como resultado da atividade humana, as concentrações desses compostos são altas. Dentre os compostos de enxofre, o dióxido de enxofre SO2 é considerado o mais prejudicial à saúde, especialmente para pessoas com dificuldade respiratória.
Adaptado de BROWN, T.L. et al, Química: a Ciência Central. 9ª ed, Ed. Pearson, São Paulo, 2007.
Em relação ao composto SO2 e sua estrutura molecular, pode-se afirmar que se trata de um composto que apresenta
Dado: número atômico S = 16 ; O = 8.
ligações covalentes polares e estrutura com geometria espacial angular.
ligações covalentes apolares e estrutura com geometria espacial linear.
ligações iônicas polares e estrutura com geometria espacial trigonal plana.
ligações covalentes apolares e estrutura com geometria espacial piramidal.
ligações iônicas polares e estrutura com geometria espacial linear.
Gabarito:
ligações covalentes polares e estrutura com geometria espacial angular.
Resolução:
O enxofre e o oxigênio possuem as seguintes distribuições eletrônicas:
16S = 1s2 2s2 2p6 3s2 3p4
8O = 1s2 2s2 2p4
Portanto, ambos possuem 6 elétrons na camada de valência, precisando de 2 para alcançar o octeto.
A estrutura de lewis, sem considerar a geometria, é:
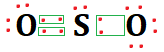
Sendo assim, o par de elétron do enxofre repulsa as ligações, levando a formação de uma geometria angular:
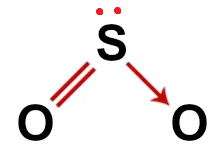
Portanto, as ligações são polares já que os átomos possuem eletronegatividade diferente, e a geometria é angular.