Questão 3
(EsPCEx 2019)
Devido ao intenso calor liberado, reações de termita são bastante utilizadas em aplicações militares como granadas incendiárias ou em atividades civis como solda de trilhos de trem. A reação de termita mais comum é a aluminotérmica, que utiliza como reagentes o alumínio metálico e o óxido de ferro III.
A reação de termita aluminotérmica pode ser representada pela equação química não balanceada:
Al (s) + Fe2O3 → Fe (s) + Al2O3 (s) + Calor
Dados: valores arredondados de entalpias padrão de formação das espécies Hºf Al2O3 = -1676 kJ/mol;
Hºf Fe2O3 = -826 kJ/mol
Acerca desse processo, são feitas as seguintes afirmativas:
I - Após correto balanceamento, o coeficiente do reagente alumínio na equação química é 2.
II - Essa é uma reação de oxidorredução e o agente oxidante é o óxido de ferro III.
III - Na condição padrão, o /Delta H da reação é -503 kJ para cada mol de óxido de alumínio produzido.
IV - Na condição padrão, para a obtenção de 56g de ferro metálico, o calor liberado na reação é de 355 kJ.
Assinale a alternativa que apresenta todas as afirmativas corretas, dentre as listadas acima.
I, II e IV.
II, III e IV.
I e II.
I e III.
III e IV.
Gabarito:
I e II.
Resolução:
Analisando cada uma das alternativas:
I - Verdadeira. Para fazer o balanceamento dessa equação:
Balanceando o alumínio:
2 Al (s) + Fe2O3 → Fe (s) + Al2O3 (s) + Calor
Balancenado o ferro:
2 Al (s) + Fe2O3 → 2 Fe (s) + Al2O3 (s) + Calor
O oxigênio já está balanceado, portanto, o coeficiente do alumínio é 2.
II - Verdadeira. Para saber se a reação é oxirredução é preciso avaliar a variação do nox:
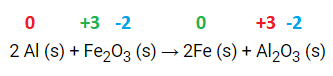
O alumínio teve o nox variado de 0 para +3, portanto, oxidou. O ferro teve o nox variado de +3 para 0, portanto, reduziu. Sendo assim, o alumínio é o agente redutor e o ferro o agente oxidante.
III - Falsa. A variação da entalpia é calculada pela fórmula:
Substituindo os dados fornecidos no enunciado:
IV - Falsa. A energia liberada de 850 kJ é para a formação de 2 mol de ferro, ou seja, 112 g. Então, o calor liberado para formar 1 mol será 425 kJ.
Considerando as afirmativas corretas, o gabarito é letra C.