Questão 9
(EsPCEx - 2019)
Neste ano de 2019, foi realizada pelos alunos da EsPCEx uma prática no laboratório de química envolvendo eletrólise com eletrodos ativos conforme a descrição experimental:
- Num béquer de capacidade 100 mL (cuba eletrolítica) coloque cerca de 50 mL de solução aquosa de sulfato de cobre II de concentração 1 mol.L-1. Tome como eletrodos uma barra fina de cobre e um prego de ferro. Ligue-os com auxílio de fios a uma fonte externa de eletricidade com uma corrente contínua de intensidade de 3 Ampères. Esta fonte tem capacidade para efetuar perfeitamente esse processo de eletrólise. O prego deve ser ligado ao polo negativo da fonte e a barra de cobre ao polo positivo da fonte. Mergulhe os eletrodos na solução durante 16 minutos e 5 segundos e observe. Considere o arranjo eletrolítico (a 25 ºC e 1 atm) e o sal completamente dissociado, conforme visto na figura a seguir:
Dado: 1 Faraday (F) = 96500 Coulomb (C) / mol de elétrons
Na discussão apresentada nos relatórios dos diversos grupos de alunos, surgiram as seguintes afirmativas:
I – Na superfície do prego ocorreu a deposição de cobre metálico.
II – Durante o processo a barra de cobre se oxida.
III – A massa de cobre metálico que se depositou na superfície do prego foi de 2,45 g.
IV – A semi-reação de redução que ocorre no cátodo é Cu+2 + 2 e- → Cu0.
V – A reação global é Fe+2 + Cu0 → Fe0 + Cu}+2.
Assinale a alternativa que apresenta todas as afirmativas corretas, dentre as listadas acima.
I, II e IV.
II, III e V.
I, IV e V.
I, II, III e IV
I, II e V.
Gabarito:
I, II e IV.
Resolução:
Na eletrólise aquosa do CuSO4, vão ocorrer as seguintes reações químicas:
Dissociação do CuSO4 ⇒ CuSO4 → Cu+2 + SO4-2
Ionização da água ⇒ 2 H2O → H3O+ + OH-
Para o polo positivo (ânodo - barra de cobre) serão direcionados as cargas negativas, ou seja, SO4-2 e OH-. Além disso, o cobre não é um eletrodo inerte, por isso, também pode oxidar. Dentre esses, o Cu tem maior facilidade de descarga (vide imagem) e por isso irá oxidar.
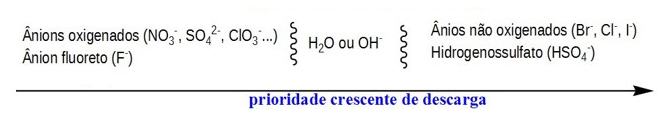
A reação de oxidação do Cu pode ser representada pela equação:
Cu → Cu+2 + 2 e-
Já no polo negativo (cátodo - prego de ferro) estarão as cargas positivas, ou seja, Cu+2 e H+. Dentre esses, o Cu+2 tem maior facilidade de descarga (vide imagem) e por isso irá reduzir.
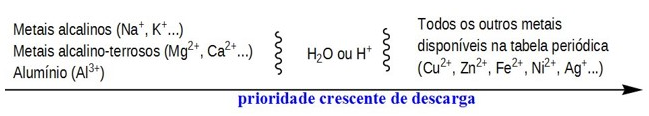
A reação de redução do Cu+2 pode ser representada pela equação:
Cu+2 + 2 e- → Cu
Analisando cada uma das afirmativas:
I - Correta. O prego de ferro está conectado ao polo negativo da bateria, por isso, atrairá as cargas positivas: Cu+2 e H+. Dentre esses, o Cu+2 irá reduzir segundo a equação Cu+2 + 2 e- → Cu, formando cobre metálico.
II - Correta. A barra de cobre está conectada ao polo positivo, portanto, irá competir na oxidação com o SO4-2 e OH-. Dentre esses, a prioridade de descarga é do cobre, que irá oxidar segundo a equação Cu → Cu+2 + 2 e-. Nesse processo oxidativo, a placa de cobre sofrerá desgaste já que o cobre metálico se transforma em Cu+2 que se encontra em solução.
III - Incorreta. Para saber a massa de cobre, considerando os dados fornecidos, utiliza-se a equação:
Sendo Q = carga [C] ; i = corrente (A); t = tempo (s).
Substituindo os valores:
De acordo com a reação de redução do cobre (Cu+2 + 2 e- → Cu), a proporção estequiométrica entre elétron e cobre metálico é 2:1, o que, considerando a massa molar do cobre, implica:
2 mol de elétron ------ 1 mol de Cu
2 mol de elétron ------ 64 g de Cu
Para relacionar a carga com a massa de cobre, é necessário saber qual a carga equivalente a 2 mol de elétron, para isso, utiliza-se o dado fornecido:
1 mol de elétron ------- 96500 C
2 mol de elétron -------- x
x = 193000 C
Portanto, a regra de três pode ser reescrita como:
193000 C ----- 64 g de Cu
Como calculado anteriormente, a carga total que passa no sistema é de 2895 C, portanto, é possível calcular a massa de Cu formada com essa carga:
193000 C ----------- 64 g de Cu
2895 C -------------- y
y = 0,96 g de Cu
Portanto, a massa de cobre metálico depositada é 0,96 g e não 2,45 g.
IV - Correta. No cátodo - polo negativo - ocorre uma disputa de descarga entre Cu+2 e H+, sendo a prioridade do Cu+2 que irá reduzir segundo a equação Cu+2 + 2 e- → Cu.
V - Incorreta. O ferro não participa da oxirredução, então não está na reação global.
Considerando apenas as afirmativas corretas, o gabarito é letra A.