Questão 59766
A tabela periódica pode ser utilizada para relacionar as propriedades dos elementos com suas estruturas atômicas; essas propriedades podem ser aperiódicas e periódicas. As propriedades periódicas são aquelas que, à medida que o número atômico aumenta, assumem valores semelhantes para intervalores regulares, isto é, repetem-se periodicamente.
O gráfico ao lado mostra a variação de uma dessas propriedades: a energia de ionização do 1º elétron, em eV, para diferentes átomos.
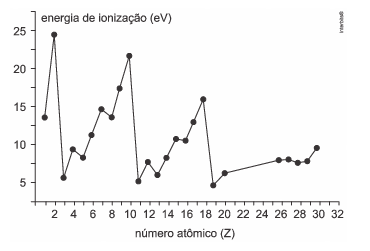
Com base no gráfico e em conhecimento em Química, responda aos itens a seguir.
a) Como se explicam os elevados valores de energia de ionização para os elementos de número atômico 2, 10 e 18?
b) No intervalo entre Z = 3 e Z = 10, observa-se aumenta da energia de ionização. Como se explica esse aumento da energia?
c) Por que o elemento de número atômico 19 apresenta o menor potencial de ionização entre os elementos representados?
d) Que número atômico, entre os elementos apresentados no gráfico, tem maior tendência a formar um ânion?
Gabarito:
Resolução:
a) Como se explicam os elevados valores de energia de ionização para os elementos de número atômico 2, 10 e 18?
Z = 2 (hélio); Z = 10 (nêonio); Z = 18 (argônio):
São todos gases nobres, por isso possuem altas energias de ionização, além disso estão mais à direita da tabela periódica, sentido em que a energia de ionização aumenta.
b) No intervalo entre Z = 3 e Z = 10, observa-se aumenta da energia de ionização. Como se explica esse aumento da energia?
O sentido de aumento da energia de ionização na tabela periódica é da esquerda para a direita, e de baixo para cima, assim quanto mais próximo do número atômico 3 (esquerda), maior é a tendência a perder elétrons, portanto, baixa energia de ionização; quanto mais próximo do número atômico 10 (direita), menor é a tendência a perder elétrons e maior a tendência de receber elétrons, consequentemente a energia de ionização é maior.
c) Por que o elemento de número atômico 19 apresenta o menor potencial de ionização entre os elementos representados?
Pois, é o que está mais abaixo e mais à esquerda na tabela periódica dos elementos representados no gráfico.
d) Que número atômico, entre os elementos apresentados no gráfico, tem maior tendência a formar um ânion?
O elemento de número atômico 9 por ter maior energia de ionização com exceção dos gases nobres.