Questão 68062
(FGV - 2012)
A tabela ao lado apresenta dados referentes às espécies K, K+, Ca2+ e S2-.
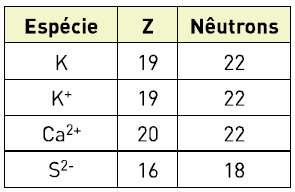
Em relação a essas espécies, são feitas as seguintes afirmações:
I. K+ e Ca2+ são isótonos.
lI. K e Ca2+ são isóbaros.
IlI. K+ tem mais prótons que K.
IV. K+ e S2- têm o mesmo número de elétrons.
É correto apenas o que se afirma em:
I e lI.
I e IlI.
I e IV.
lI e IlI.
lI e IV.
Gabarito:
I e IV.
Resolução:
Isótonos: átomos com mesmo número de nêutrons.
Isobáros: átomos com mesmo número de massa (A) e diferente número atômico (Z).
I. K+ e Ca2+ são isótonos.
Correto. Ambos tem o mesmo número de nêutrons (22).
lI. K e Ca2+ são isóbaros.
Incorreto.
• Cálculo da massa de K
A = n + Z
A = 22 + 19 = 41
• Cálculo da massa de Ca2+
A = n + Z
A = 22 + 20= 42
Como o K e o Ca2+ não possuem mesmo número de massa, eles não são isóbaros.
IlI. K+ tem mais prótons que K.
Incorreto.
K+ é um cátion formado quando um átomo de K perde 1 elétron. As duas espécies possuem o mesmo número de prótons.
IV. K+ e S2- têm o mesmo número de elétrons.
Correto.
Como o átomo é uma espécie neutra, o número de elétrons de um átomo é igual ao número de prótons que, por sua vez, é igual ao número atômico (Z).
O número de prótons e o número de elétrons de um átomo de K é 19. O cátion K+ é formado quando um átomo de K perde 1 elétron. Portanto, o número de elétrons do cátion K+ é 18.
O número de prótons e o número de elétrons de um átomo de S é 16. O ânion S2- é formado quando um átomo de S recebe 2 elétrons. Portanto, o número de elétrons do ânion S2- é 18.
As duas espécies são isoeletrônicas.