Questão 2
(FUVEST 2012 - 2ª fase)
Um aluno efetuou um experimento para avaliar o calor envolvido na reação de um ácido com uma base. Para isso, tomou 8 tubos de ensaio e a cada um deles adicionou 50 mL de uma mesma solução aquosa de HCl e diferentes volumes de água. Em seguida, acondicionou esses tubos em uma caixa de isopor, para minimizar trocas de calor com o ambiente. A cada um desses tubos, foram adaptados uma rolha e um termômetro para medir a temperatura máxima atingida pela respectiva solução, após o acréscimo rápido de volumes diferentes de uma mesma solução aquosa de NaOH. O volume final da mistura, em cada tubo, foi sempre 100 mL. Os resultados do experimento são apresentados na tabela.
a) Construa um gráfico, no quadriculado apresentado na página de resposta, que mostre como a temperatura máxima varia em função do volume de solução aquosa de NaOH acrescentado.
b) A reação do ácido com a base libera ou absorve calor? Justifique sua resposta, considerando os dados da tabela.
c) Calcule a concentração, em mol L-1, da solução aquosa de HCl, sabendo que a concentração da solução aquosa de NaOH utilizada era 2,0 mol L-1.
Gabarito:
Resolução:
a)
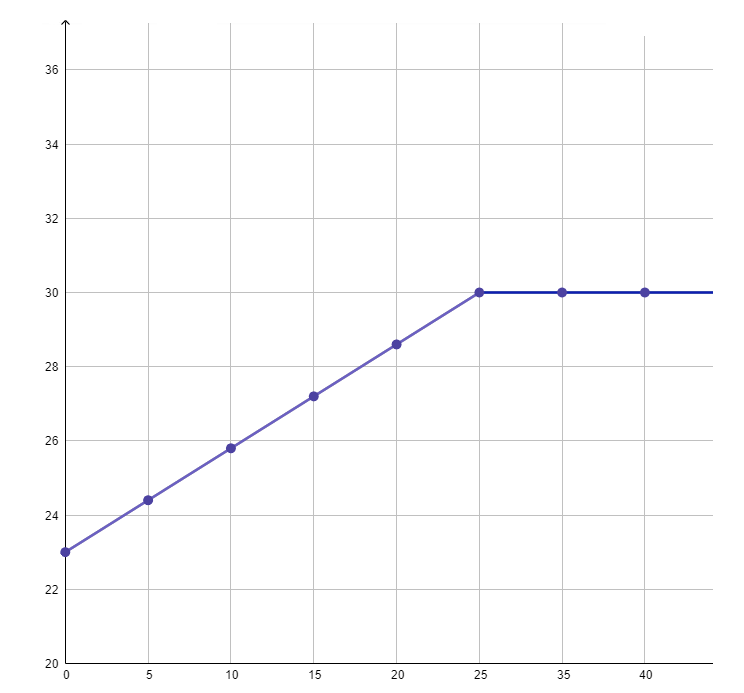
b) A reação do ácido com a base libera calor. Os dados da tabela mostram que a adição da solução de NaOH à solução de HCl aumenta a temperatura do sistema.
c) No momento em que a temperatura para de variar, a reação para de acontecer. A temperatura máxima de 30ºC é atingida no volume de base de 25 mL. Portanto, para neutralizar 50 mL da solução de HCl foram necessários 25 mL da solução de NaOH 0,2 molL-1.
Equação da reação entre o ácido clorídrico e o hidróxido de sódio
HCl(aq) + NaOH(aq) → Na+(aq) + Cl-(aq) + H2O(l)
Como a estequiometria da reação é de 1:1, pode-se escrever a seguinte relação entre as quantidades de matéria de ácido e de base no ponto de equivalência
(equação 1)
A concentração é definida como a razão entre a quantidade de matéria e o volume
então pode-se substituir a quantidade de matéria (n) na equação 1:
Como o volume de HCl é o dobro do volume de NaOH: