Questão 10541
(FUVEST - 2017)
Sob certas condições, tanto o gás flúor quanto o gás cloro podem reagir com hidrogênio gasoso, formando, respectivamente, os haletos de hidrogênio HF e HC , gasosos. Pode-se estimar a variação de entalpia (ΔH) de cada uma dessas reações, utilizando-se dados de energia de ligação. A tabela apresenta os valores de energia de ligação dos reagentes e produtos dessas reações a 25 °C e 1atm.
Com base nesses dados, um estudante calculou a variação de entalpia (ΔH) de cada uma das reações e concluiu, corretamente, que, nas condições empregadas,
ambas as reações são endotérmicas.
Gabarito:
a formação de HF(g) é a reação que libera mais energia.
Resolução:
Pode-se obter a variação de entalpia da reação pelos valores de energia de ligação dos reagentes e produtos:
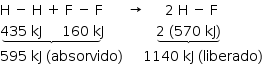
Como a energia liberada é maior que a absorvida, a reação é exotérmica, e o valor do ΔH é –545 kJ.
A mesma coisa pode ser feita para a reação de formação de HCl.
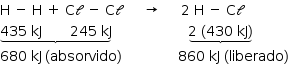
Assim como na reação acima, a energia liberada é maior que a energia absorvida, temos uma reação exotérmica, e o valor do ΔH é –180 kJ.