Questão 61015
(FUVEST - 2007 - Adaptada)
Considere as seguintes equações químicas:
I. H2 + F2 → 2 HF
II. HF + H2O → H3O+ + F-
III. 2 Na0 + F2 → 2 Na+F-
IV. HF + NH3 → NH4+F-
a) Reescreva as equações utilizando estruturas de Lewis (fórmulas eletrônicas em que os elétrons de valência são representados por • ou x), tanto para os reagentes quanto para os produtos.
b) Faça uma análise comparativa dos pontos de fusão e ebulição dos produtos das equações I e III. Justifique a diferença entre eles.
Gabarito:
Resolução:
a)
I:
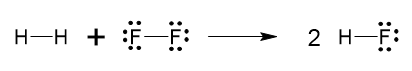
II:
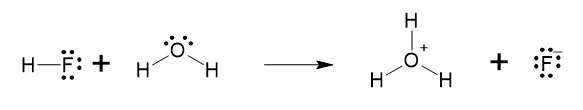
III:
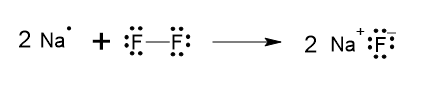
IV:
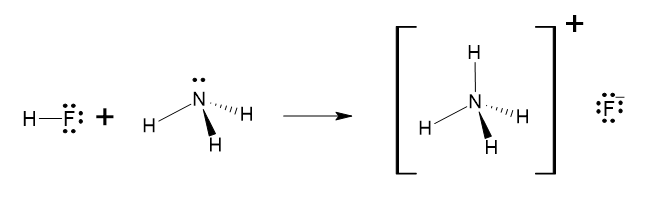
b) As interações entre as moléculas de HF são interações dipolo-dipolo (que chamamos de ligações de hidrogênio quando o átomo ligado ao hidrogênio é muito eletronegativo), enquanto as interações entre os íons que compõem a estrutura do NaF são ligações iônicas. Como as ligações iônicas são mais fortes do que as interações dipolo-dipolo, a quantidade de energia necessária para promover a mudança de estado físico do NaF é maior do que a quantidade de energia necessária para promover a mudança de estado físico do HF e por isso as temperaturas de fusão e ebulição do NaF são maiores que as do HF.
*A adaptação foi feita com a adição da letra b que não está presente no vestibular original