Questão 5
[IME- 2012/2013 - 2ª fase]
O poli(vinil-butiral) ou PVB é produzido a partir do poli(acetato de vinila) ou PVA em duas etapas. Na primeira, ocorre a alcóolise básica do PVA com metanol, gerando um precipitado de poli(álcool vinílico) ou PVAl. Na segunda, o PVAl dissolvido em água quente reage com butanal na presença de ácido sulfúrico, dando origem a um precipitado de PVB, cujo mero (estrutura que se repete) não possui hidroxila livre.
a) Escreva as fórmulas estruturais dos polímeros I e II da rota sintética abaixo.
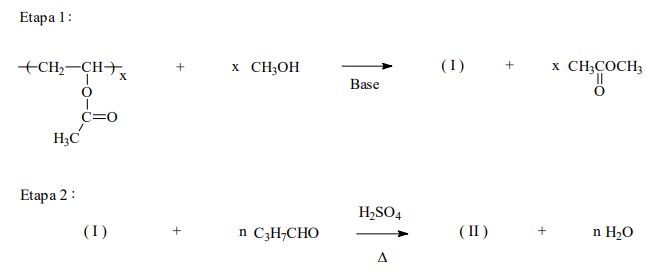
b) Num processo de bancada, similar ao descrito anteriormente, utilizam-se 174 g de um PVAl que apresenta razão . Sabendo-se que 24% das hidroxilas reativas deste PVAl permanecerão inertes, gerando-se assim, em (II), um copolímero de PVAl e PVB, determine a fração mássica de PVB no copolímero formado.
Gabarito:
Resolução:
a)
Na primeira, ocorre a alcóolise básica (ou transesterificação) do PVA com metanol.

(I) =

Na segunda etapa (I) pode ser escrito como:

Assim conseguimos mostrar que é um diol, e o composto pode sofrer reações como tal, ou seja, sofrer adição de carbonila para formar um cetal cíclico. O que pode ser representado de forma simplificada:

(II) =

b)
Cada 58g de PVAI temos 1 mol de OH-
Em 174g temos x mol de OH-
O monômero do PVAI:

Poaaui 44g/mol, dessa forma em 174g de polímero temos:
y = 3,95 repetiçoes do monômero.
Como cada mol do monômero possui 1 mol de hidroxila, os 3 mols de hidroxila reativos não são correspondem ao total de mols do polímero.
Desses 3 mols de hidroxila reativos, 24% (0,72 mol) não reagiram e 76% (2,28 mol) reagiram.
Para formar o monômero do PVB são necesários 2 hidroxilas, com isso, como 2,28 mol reagira, 1,14 mol do monômero do PVB foram formados. 1 mol desse monômero tem massa de 142g/mol.
z = 161,88 g do monômero são formados.
Como a proporção do monômero do PVB com o butanal e com a água é de 1:1, 1,14 mol reagem com 1,14 mol de butanal e 1,14 mol de água.
Sabendo que a massa molar do butanal e da água são respectivamente 72g/mol e 18g/mol, portanto a massa adicionada ao polímero foi de:
Temos então a razão