Questão 24866
[IME- 2012/2013 - Adaptação]
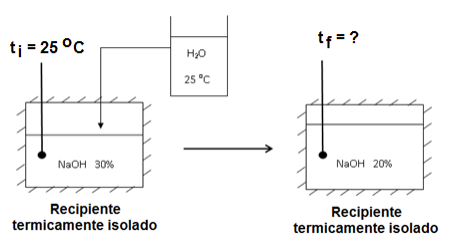
Considere um recipiente adiabático conforme a ilustração abaixo, no qual 1000g de uma solução aquosa de NaOH, a 30% em massa, e a uma temperatura inicial ti = 25 ºC, são diluídos a 20% em massa, com água à mesma temperatura.
Calcule a temperatura tr da solução após a diluição.
Dados:
- Para o sistema NaOH – água a 25 ºC:
a 30% : H = 104 J/g de solução; cP = 3,54 J.g–1 . ºC–1
a 20% : H = 76 J/g de solução; cP = 3,63 J.g–1 . ºC–1
- Calor específico da água líquida: cP = 4,18 J.g–1 . ºC–1
- Estado de referência para entalpia: água líquida a 0 ºC
Calcule a temperatura tr da solução após a diluição
27,4 ºC
30,2 ºC
32,8 ºC
35,0 ºC
38,6 ºC
Gabarito:
32,8 ºC
Resolução:
A entalpia padrão dada foi da água líquida à 0 ºC, então a entalpia da água líquida à 0 ºC deve ser 0.
Logo, a entalpia da água à 25 ºC deve ser o calor absorvido por ela para sofre o aquecimento:
HH2O 25ºC = 1 g * 4,18 J/g.ºC * (25 - 0) ºC = 104,5 J para cada grama de água.
Para diluir a solução de 1000 gramas com 30% em massa para uma solução de 20% em massa, é preciso acrescentas m gramas de água:
Nas 1000 gramas de solução inicial devemos ter 30% em massa da base, isto é, temos 300 gramas da base.
Os mesmo 300 gramas de base permanecem ao diluir a solução, contudo são adicionados m gramas de água e a porcentagem em massa passa a ser de 20%:
%m/m = 0,2 = mbase/msolução = 300 g/(1000 g + m)
Resolvendo, temos que m = 500 g.
Sendo assim, a entalpia final da solução após adicionar a água deve ser:
Hsolução 30% + HH2O 25ºC = 104 J/g * 1000 g + 104,5 J/g * 500 g = 156250 J (I)
Essa entalpia deve ser igual a entalpia da solução 20% em massa na temperatura de 25 ºC mais uma quantidade de calor responsável pelo aquecimento dessa solução (durante a diluição) até a temperatura T:
Hsolução 20% + Q = 76 J/g * 1500 g + 1500 g * 3,63 J/g.ºC * (T - 25) ºC (II)
Igualando (I) e (II), temos:
156250 = 76*1500 + 1500* 3,63* (T - 25)
Resolvendo a equação, temos que T = 32,8 ºC