Questão 36
[IME - 2013/2014 - 1ª fase]
Um experimento clássico indica que o oxigênio molecular (O2) exibe propriedades magnéticas no seu estado fundamental. O experimento consiste em fazer passar oxigênio líquido pelos polos de um ímã. Observa-se que o oxigênio fica retido, como mostra a figura a seguir:
Nas alternativas abaixo, são apresentados os orbitais 2p de dois átomos de oxigênio e o spin dos elétrons que ocupam seus orbitais atômicos. Também são apresentadas possíveis interações químicas que podem resultar em ligações químicas estabelecidas entre esses dois átomos. Considerando a observação experimental e os requisitos eletrônicos e energéticos para o estabelecimento de ligações químicas, indique qual das alternativas abaixo representa melhor o O2 no estado fundamental.
NDA
Gabarito:
NDA
Resolução:
A questão demonstra um experimento clássico no qual o oxigênio molecular líquido fica retido entre dois polos de um imã. Este experimento demonstra que o oxigênio exibir propriedades magnéticas característica apresentada por um composto paramagnético (que possui elétrons desemparelhados). A apresentação do referido experimento nos induz a aplicação da teoria dos orbitais moleculares, única teoria capaz de explicar satisfatoriamente o paramagnetismo apresentado pelo O2. Como enunciado da questão pede para considerarmos a observação experimental, nenhuma representação apresentada (as quais consideram a teoria de ligação de Valência, representando os orbitais atômicos) pode representar corretamente a estrutura de ligação do O2, abaixo demonstraremos como todas as alternativas mostradas apresentam-se incorretas, depois apresentaremos a representação correta.
a) Errada. A representação sugere apenas a formação de uma ligação simples (ligação ) e sabemos que o O2 faz uma ligação dupla (ligação
+ ligação
). A ligação
neste caso não pode ser estabelecida, pois os elétrons presentes no orbital py encontram-se desemparelhadas (spins semelhantes). A ligação
é aquela formada pela sobreposição frontal dos orbitais (ao longo do eixo de ligação, neste caso o eixo Z), enquanto a ligação
é formada pela sobreposição lateral dos orbitais (eixo Y eixo X).
b) Errada. A ligação apresentada está incorreta, pois ocorre entre dois elétrons desemparelhados (spins semelhantes) o que não é possível. Outro erro na questão e ausência da ligação
já que o O2 apresenta uma ligação dupla.
c) Errada. A representação explica a formação da ligação dupla segunda teoria de Valência, como vemos pela figura todos os elétrons estão emparelhados, logo a representação não é capaz de explicar o paramagnestismo do O2.
d) Errada. A representação demonstra apenas a formação de uma ligação simples (ligação ) e sabemos que no O2 a uma ligação dupla (ligação
+ ligação
).
e) Errada. A representação sugere a formação de uma ligação dupla constituída de ligações , o que não é correto uma ligação dupla é formado por uma ligação
mais uma ligação
.
Assim a melhor representação para o O2, que explica o paramagnetistmo, seria dado pela Teoria do Orbital Molecular, onde é o orbital molecular sigma ligante;
é um orbital molecular sigma antiligante;
é orbital molecular pi ligante;
é um orbital molecular pi antiligante.
O correto seria então:
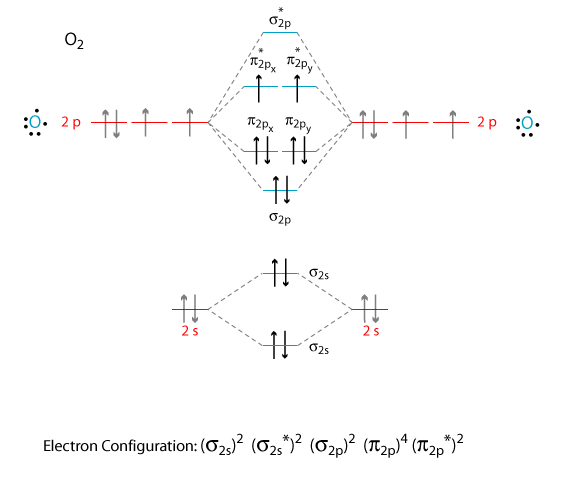
Onde podemos ver os dois elétrons desemparelhados que é o que possibilita o paramagnetismo do O2.