Questão 1
(IME 2022/2023 - 2ª fase)
Considere:
- Constante universal dos gases ideais:
- Constante de Faraday =
= 1,3×10−8
- Composicão molar do ar atmosférico: 79% de N2 e 21% de O2
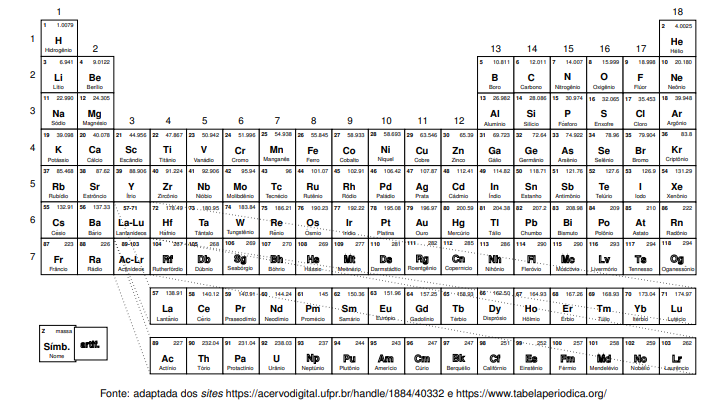
Tabela Periodica dos Elementos Químicos:
O calcário é uma rocha de origem sedimentar constituída predominantemente por carbonato de cálcio. Uma técnica que pode ser utilizada para determinar o teor de carbonato de cálcio em uma amostra de calcário é a volumétria, a qual consiste na determinação da concentração de uma solução A por meio do gasto de uma solução B de concentração conhecida, ocorrendo uma reação química entre A e B.
Uma amostra de 1,0 g de calcário foi dissolvida utilizando-se 25,0 mL de uma solução de ácido clorídrico com concentração de 1,0 mol/L. Na sequência, utilizou-se uma solução de hidróxido de sódio com concentração de 0,5 mol/L para neutralizar o excesso de ácido, consumindo-se 17,2 mL da solução.
Considerando que apenas o carbonato de cálcio presente na amostra de calcário reage com o ácido clorídrico, determine:
a) as equações balanceadas das reações envolvidas no processo;
b) a porcentagem mássica de carbonato de cálcio presente na amostra de calcário.
Gabarito:
Resolução:
A)
Reação de tratamento: (I)
Titulação: (II)
B)
Quantidade em excesso do é o que vai reagir com o
, assim, pela reação II:
De acordo com a reação I:
Logo, .