Questão 7
(IME 2022/2023 - 2ª fase)
Considere:
- Constante universal dos gases ideais:
- Constante de Faraday =
= 1,3×10−8
- Composicão molar do ar atmosférico: 79% de N2 e 21% de O2
Tabela Periódica dos Elementos Químicos:
Considere a energia potencial de ligação. Pode-se imaginar um modelo em que a energia de ligação entre as espécies seja considerada a própria energia potencial eletrostática.
a) Esboce, em um único gráfico de energia potencial de ligação versus distância internuclear, as curvas para uma ligação química interatômica (covalente ou iônica) e para uma interação intermolecular.
b) Indique o fator crucial que determina a diferença entre as curvas.
Gabarito:
Resolução:
A)
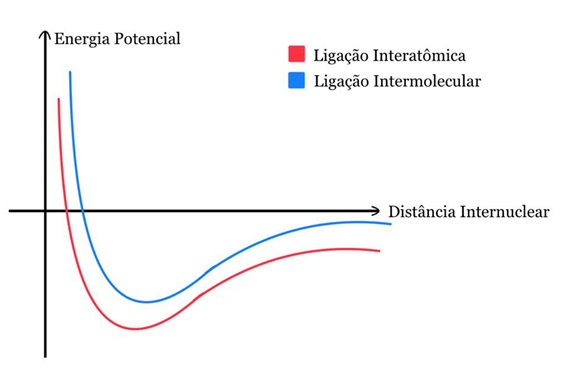
B) Com a superposição dos orbitais para a formação de orbitais moleculares, há uma liberação maior de energia, por isso, em uma ligação química, a energia é liberada em maior quantidade. A energia potencial elétrica mínima é menor na ligação interatômica.