Questão 682
(ITA - 2012 - 1ª Fase)
Considere que a reação hipotética representada pela equação química X + Y Z ocorra em três condições diferentes (a, b e c), na mesma temperatura, pressão e composição total (número de moléculas de X + Y), a saber:
a) O número de moléculas de X é igual ao número de moléculas de Y.
b) O número de moléculas de X é 1/3 do número de moléculas de Y.
c) O número de moléculas de Y é 1/3 do número de moléculas de X.
Baseando nestas informações, considere que sejam feitas as seguintes afirmações:
I. Se a lei de velocidade da reação for v = k[X]|Y]2, então vc < va < vb .
II. Se a lei de velocidade da reação for v = k[X][Y], então vb = vc < va .
III. Se a lei de velocidade da reação for v = k[X], então t1/2(c) > t1/2(b) > t1/2(a), em que t1/2 = tempo de meia-vida.
Das afirmações acima, está(ão) CORRETAS(s) apenas
I.
I e II.
II.
II e III.
III.
Gabarito:
I e II.
Resolução:
a) A partir das informações, teremos:
n: número total de mols; nX = nY.
b) n = nX + nY
c) n = nX + nY
I. Correto. Se a lei de velocidade da reação for v = k[X]|Y]2, então vc < va < vb .
II. Correto. Se a lei de velocidade da reação for v = k[X][Y], então vb = vc < va .
III. Incorreto. Se a lei de velocidade da reação for v = k[X], então t1/2(c) > t1/2(b) > t1/2(a), em que t1/2 = tempo de meia-vida.
v = K [X] representa uma reação de primeira ordem.
Nas reações de primeira ordem os tempos de meia-vida são iguais, já que a velocidade e concentração de X são lineares.
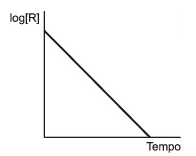
Como loge = 2,303 log, multiplicando a equação:
No tempo de meia-vida a concentração do reagente cai pela metade, ou seja, [R] = [R]0/2. Substituindo na equação acima, vem: