Questão 18834
(Pucrs 2014) Em temperatura ambiente, colocou-se uma porção de palha de aço, previamente lavada com ácido acético para remoção de óxidos, no fundo de uma proveta. Imediatamente, colocou-se a proveta emborcada em um copo com água. Observou-se, após cerca de 30 minutos, que a água aumentou de volume dentro da proveta, conforme ilustração.
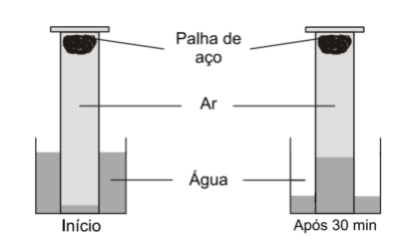
A hipótese mais provável para explicar o ocorrido é que
parte do ar dissolveu-se na água, fazendo com que a água ocupasse o lugar do ar dissolvido.
o ar contraiu-se pela ação da pressão externa.
79% da quantidade de ar reagiu com a palha de aço.
parte da água vaporizou-se, pois o sistema está à temperatura ambiente.
o oxigênio presente no ar reagiu com o ferro da palha de aço, formando óxido de ferro.
Gabarito:
o oxigênio presente no ar reagiu com o ferro da palha de aço, formando óxido de ferro.
Resolução:
Sabemos que em temperatura ambiente, colocou-se uma porção de palha de aço, previamente lavada com ácido acético para remoção de óxidos, no fundo de uma proveta. Imediatamente depois, colocou-se a proveta emborcada em um copo com água. Após cerca de 30 minutos, que a água aumentou de volume dentro da proveta.
O que aconteceu foi uma reação de oxido - redução, onde o oxigênio do ar, presente no sistema, reagiu com o ferro da palha, oxidando-o, e formando ferrugem, ou seja, óxido de ferro e reduzindo o oxigênio.
Enquanto a água entrou na proveta, e ocupou o volume o espaço que antes ocupada o oxigênio.