Questão 70936
(UEA - 2020)
Considere a célula galvânica representada e as semirreações com os seus valores de potenciais-padrão de redução a 25 ºC e 1 atm.
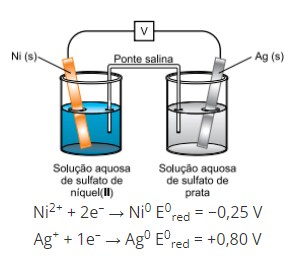
O valor da diferença de potencial dessa célula galvânica e o metal que constitui o cátodo são
+0,55 V e níquel.
–1,05 V e níquel.
+1,05 V e níquel.
+1,05 V e prata.
–0,55 V e prata.
Gabarito:
+1,05 V e prata.
Resolução:
Ni2+ + 2e- → Ni0 E0red = -0,25V
Ag+ + 1e- → Ag0 E0red = +0,80V
Invertendo a semirreação do níquel temos:
Ni0 → Ni2+ + 2e- E0oxi = +0,25V
Ag+ + 1e- → Ag0 E0red = +0,80V
O potencial total da reação será +0,25 + 0,80 = + 1,05 V
E quem reduziu foi a prata, portanto ela será o cátodo.