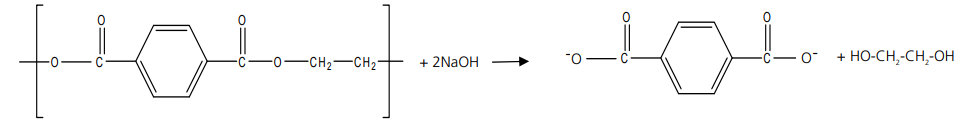Questão 22
(UNICAMP - 2012 - 2 fase - Questão 6)
A questão ambiental relativa ao destino de plásticos utilizados é bastante antiga e algumas propostas têm sido feitas para contornar esse problema. A mais simples é a queima desses resíduos para aproveitamento da energia, e outra é o seu reuso após algum tratamento químico. Para responder aos itens a e b, considere a estrutura abaixo como um fragmento (C10H8O4) representativo do PET.
a) Levando em conta a equação de combustão completa do fragmento do PET, calcule a energia liberada na queima de uma garrafa PET de massa igual a 48 gramas.
b) No tratamento químico da embalagem PET com solução de hidróxido de sódio ocorre uma reação de hidrólise que remove uma camada superficial do polímero, e que permite a reutilização da embalagem. Com base nessas informações complete a equação química de hidrólise do fragmento de PET, no espaço de respostas.
Dados de entalpia de formação em kJ mol-1: fragmento = -476; CO2 = -394; H2O = -286.
Gabarito:
Resolução:
a) Equação da reação de combustão do fragmento:
C10H8O4 + 10 O2 → 10 CO2 + 4 H2O
Cálculo da entalpia padrão de combustão:
Esse é o valor da energia liberada por mol de fragmento. A massa molar de C10H8O4 é 192 gmol-1. A energia liberada na combustão de 48g pode ser calculada pela relação
| 192 g C10H8O4 | __________ | -4608 kJ |
| 48 g C10H8O4 | __________ | x |
x = -1152 kJ
b)
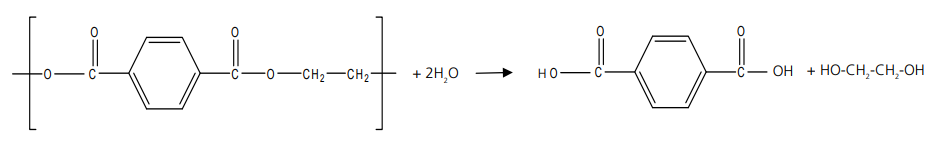
Como a reação ocorre em meio básico, a equação química também poderia ser escrita como