Questão 22
(UNICAMP - 2022 - 1ª fase - Caderno R)
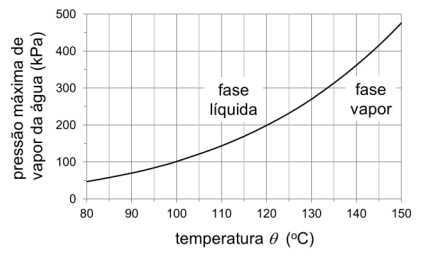
A autoclave, um equipamento de esterilização de objetos por meio de vapor de água em alta temperatura e pressão, foi inventada por Charles Chamberland, a pedido de Louis Pasteur. A figura a seguir mostra a curva da pressão máxima de vapor da água em função da temperatura. Para temperaturas e pressões do lado esquerdo da curva, a água encontra-se na fase líquida; do lado direito, a água está na fase de vapor. Nos pontos sobre a curva, as fases líquida e de vapor coexistem. A pressão de funcionamento de uma determinada autoclave é p = 3,0 atm. Se toda a água está na fase de vapor, o que se pode dizer sobre a sua temperatura ?
Dado: 1,0atm = 100 kPa
pode ter qualquer valor maior que 100 ºC
pode ter qualquer valor maior que 100 ºC e menor que 133 ºC
pode ter qualquer valor menor que 100 ºC ou maior que 133 ºC
pode ter qualquer valor maior que 133 ºC.
Gabarito:
pode ter qualquer valor maior que 133 ºC.
Resolução:
Pelo gráfico podemos perceber que para que a água esteja totalmente na fase de vapor, ela deve-se encontrar abaixo da curva. Com isso sabendo que 3atm=300kPa traçamos a seguinte reta
Logo a temperatura deve ser maior que 133°C. Perceba que o valor só pôde ser estimado com tamanha certeza devido às alternativas, pelo “olhometro” sabemos que é um valor próximo ao 135°C.
Alternativa D.