Questão 44720
FUVEST
(FUVEST 2012 - 2ª fase)
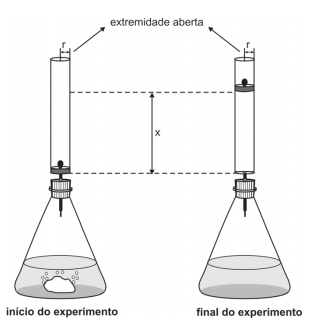
A um recipiente, contendo solução aquosa de ácido sulfúrico, foi adicionada uma massa m de carbonato de sódio. Imediatamente após a adição desse sal, foi adaptado, à boca do recipiente, um cilindro de raio r, no interior do qual um êmbolo, de massa desprezível, pode se deslocar sem atrito. Após algum tempo, o carbonato de sódio foi totalmente consumido, e o gás liberado moveu o êmbolo para cima. Nessa transformação, o ácido sulfúrico era o reagente em excesso.
a) Escreva a equação química balanceada que representa a transformação que ocorreu dentro do recipiente.
b) O experimento descrito foi repetido utilizando-se carbonato de potássio em lugar de carbonato de sódio. A massa de carbonato de potássio utilizada nesse segundo experimento também foi m. A altura atingida pelo êmbolo foi a mesma nos dois experimentos? Explique. (Considere desprezível a variação de temperatura no sistema).
c) Escreva a expressão matemática que relaciona a altura x, atingida pelo êmbolo, com a massa m de carbonato de sódio.
Para isso, considere que
- a solubilidade do gás, na solução, é desprezível, e não há perda de gás para a atmosfera;
- nas condições do experimento, o gás formado se comporta como um gás ideal, cujo volume é dado por V = nRT/P, em que:
P = pressão do gás
n = quantidade de matéria do gás (em mol)
R = constante universal dos gases
T = temperatura do gás (em K)
Observação: Use a abreviatura MM para representar a massa molar do carbonato de sódio.
Gabarito:
Resolução:
a)
H2SO4(aq) + Na2CO3(aq) → Na2SO4(aq) + H2CO3(aq)
O ácido carbônico é uma espécie instável e se decompõe em água e gás carbônico. Portanto, a reação entre ácido sulfúrico e carbonato de sódio pode ser representada pela equação
H2SO4(aq) + Na2CO3(aq) → Na2SO4(aq) + H2O(l) + CO2(g)
b)
O deslocamento do êmbolo ocorre devido à formação do gás carbônico. A quatidade de gás formado é maior quanto maior for a quantidade de matéria (em mol) do carbonato.
Os carbonatos de sódio e potássio têm fórmulas Na2CO3 e K2CO3, respectivamente. A massa molar é definida como a razão entre a massa e a quantidade de matéria
e a quantidade de matéria pode ser calculada por
Como a massa molar do potássio é maior que a massa molar do sódio, para a mesma massa m dos dos sais, a quantidade de matéria n do carbonato de potássio é menor do que a do carbonato de sódio. Portanto, a quantidade de gás formado na reação entre carbonato de potássio e ácido sulfúrico é menor do que na reação que utiliza o carbonato de sódio.
c)
Equação dos gases ideais
A proporção estequiométrica entre o carbonato de sódio e o gás carbônico é 1:1. Pode-se escrever a equação dos gases ideais utilizando a quantidade de matéria (n) do carbonato de sódio:
O volume do cilindro é dado por
Portanto, a expressão que relaciona a altura x e a massa de carbonato de sódio m é