Questão 13
(EsPCEx - 2011)
Um antiácido estomacal contém bicarbonato de sódio (NaHCO3) que neutraliza o excesso de ácido clorídrico (HCl) no suco gástrico, aliviando os sintomas da azia, segundo a equação:
HCl(aq) + NaHCO3(aq) → NaCl(aq) + H2O(l) + CO2(g)
Sobre essas substâncias, são feitas as seguintes afirmações:
I. A fórmula estrutural do bicarbonato de sódio e do ácido clorídrico são respectivamente:
II. Na reação entre o bicarbonato de sódio e o ácido clorídrico, ocorre uma reação de oxidorredução.
III. O antiácido contém 4,200 g de bicarbonato de sódio para neutralização total de 1,825 g do ácido clorídrico presente no suco gástrico.
Dados:
Das afirmações feitas, está(ão) correta(s)
apenas I e II.
apenas II e III.
apenas I e III.
apenas III.
apenas II.
Gabarito:
apenas III.
Resolução:
I. Incorreta. Na fórmula do íon bicarboanto (HCO3-) representada na afirmativa, o carbono faz cinco ligações. Na fórmula do HCl, os átomos de hidrogênio e cloro fazem duas ligações. As estruturas corretas das espécies estão representadas abaixo:
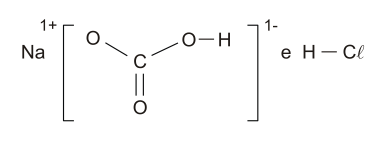
II. Incorreta. Equação da reação entre o bicarbonato de sódio (NaHCO3) e o ácido clorídrico (HCl):
NaHCO3(aq) + HCl(aq) → NaCl(aq) + H2O(l) + CO2(g)
Não ocorre variação no número de oxidação de nenhum dos átomos, então esta não é uma reação de oxirredução.
III. Correta.
O antiácido contém 4,200 g de bicarbonato de sódio para neutralização total de 1,825 g do ácido clorídrico presente no suco gástrico.
• Cálculo da massa molar de NaHCO3:
MMNaHCO3 = MMNa + MMH + MMC + 3 x MMO
MMNaHCO3 = 23 + 1 + 12 + 3 x 16
MMNaHCO3 = 84 g.mol-1
• Cálculo da massa molar de HCl:
MMHCl = MMH + MMCl
MMHCl = 1 + 35,5
MMHCl = 36,5 g.mol-1
Pela proporção estequiométrica da reação, 1 mol de NaHCO3 (84g) reage completamente com 1 mol de HCl (36,5g). Portanto, a massa de bicarbonato de sódio necessária para neutralizar 1,825g de ácido clorídrico é:
| 84g NaHCO3 | __________ | 36,5g HCl |
| mNaHCO3 | __________ | 1,825g HCl |