Questão 44770
(FUVEST - 2007 - 2 fase - Questão 4)
Na produção de hidrogênio por via petroquímica, sobram traços de CO e CO2 nesse gás, o que impede sua aplicação em hidrogenações catalíticas, uma vez que CO é veneno de catalisador. Usando-se o próprio hidrogênio, essas impurezas são removidas, sendo transformadas em CH4 e H2O. Essas reações ocorrem a temperaturas elevadas, em que reagentes e produtos são gasosos, chegando a um equilíbrio de constante KI no caso do CO e a um equilíbrio de constante KII no caso do CO2. O gráfico traz a variação dessas constantes com a temperatura.
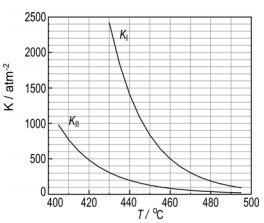
a) Num experimento de laboratório, realizado a 460 oC, as pressões parciais de CO, H2, CH4 e H2O, eram, respectivamente, 4 x 10-5 atm; 2 atm; 0,4 atm; e 0,4 atm. Verifique se o equilíbrio químico foi alcançado. Explique.
b) As transformações de CO e CO2 em CH4 mais H2O são exotérmicas ou endotérmicas? Justifique sua resposta.
c) Em qual das duas transformações, na de CO ou na de CO2, o calor desprendido ou absorvido é maior? Explique, em termos do módulo da quantidade de calor envolvida.
Gabarito:
Resolução:
a) CO(g) + 3H2(g) ----> CH4(g) + H2O(g)
A partir da equação e das pressões fornecidas, podemos calcular o quoeficiente reacional Qp:
Ao analisar o gráfico, pode-se concluir que Qp = Kl, e portanto o sistema está em equilíbrio.
b) A partir do gráfico podemos concluir que tanto para reação I como para a reação II o aumento da temperatura implica em uma diminuição da constante de equilíbrio, e por isso ambas as reações são exotérmicas.
c) A reação I apresenta maior valor para a constante de equilíbrio que a reação II,para uma mesma temperatura, o que indica que a reação I é mais espontânea. Levando em conta apenas a entalpia, a reação I libera mais calor.