Questão 76
(FUVEST- 2022 - 1ª fase)
O hidróxido de alumínio (Al(OH)3), ao precipitar em solução aquosa, forma um sólido gelatinoso que pode ser usado como agente floculante no tratamento de água. Essa precipitação pode ocorrer pela adição de um hidróxido solúvel a uma solução aquosa ácida contendo um sal de alumínio solúvel, como o AlCl3. Entretanto, adicionando-se excesso de hidróxido ao meio, há a formação de íons Al(OH)4-, espécie solúvel em água, e o precipitado se solubiliza novamente. Dessa forma, dependendo do pH do meio, uma dentre as espécies Al(OH)4-(aq), Al(OH)3(s) e Al3+(aq) estará presente na solução em quantidade maior que as demais, como exemplificado no esquema.
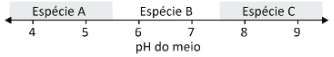
A alternativa que mostra corretamente qual das espécies estará em quantidade maior que as duas outras em cada faixa de pH é:

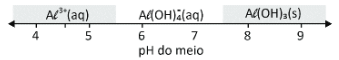
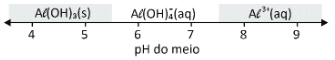
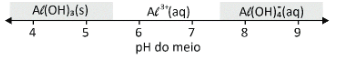
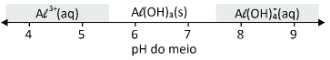
Gabarito:
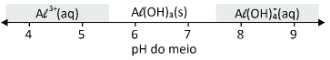
Resolução:
Segundo o enunciado, a precipitação do Al(OH)3 vai ocorrer devido a adição de um hidróxido que seja solúvel na água, liberando íons OH-, a uma solução (em meio ácido) que contém AlCl3, também solúvel e que vai liberar íons Al3+. Além disso, a questão também nos fala que, em excesso de hidróxido (meio básico), haverá formação de íons Al(OH)4-.
Pelo que foi dito, podemos assumir que:
► Em meio ácido, teremos a neutralização desse meio pelos íons hidróxidos liberados no meio, fazendo com que haja excesso de íons Al3+ que não reagiram.
► Em pH neutro, ocorre a reação proporcional dos íons Al3+ e OH- que vão formar o hidróxido de alumínio (Al(OH)3).
► Em meio básico, como foi dito no enunciado, teremos excesso de íons Al(OH)4- devido a adição de íons hidróxido maiores que o necessário.
Pelas alternativas, a que melhor se encaixa com a situação será: