Questão 5
(FUVEST - 2022 - 2ª FASE)
Nas vias públicas, é possível encontrar totens conforme os representados na figura. Em um deles há a inscrição “COMGAS”, indicando que ali passa um gasoduto da empresa distribuidora de gás; no outro está escrito “PROT CATÓDICA”, o que indica que há uma proteção catódica no gasoduto.

Sabendo que o gasoduto é constituído de aço, responda:
a) No sistema do gasoduto apresentado, o gasoduto é o ânodo ou o cátodo da célula eletroquímica? Justifique a sua resposta.
b) Considere os seguintes potenciais de redução dos metais (ɛ°):
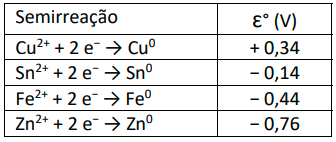
Qual(is) desses metais pode(m) ser utilizado(s) para a proteção catódica do gasoduto? Esse(s) metal(is) será(ão) o polo positivo ou negativo da célula eletroquímica?
c) Considere que a composição molar do gás transportado pelo gasoduto Brasil-Bolívia é de, aproximadamente, 93,5% metano, 4,1% etano e 2,4% N2. Calcule a massa, em kg, de etano existente em uma seção de 1 m3 do duto sabendo que a pressão no interior do duto é de 100 atm à temperatura de 27 °C. Apresente os cálculos.
|
Note e adote: Constante universal dos gases ideais: R = 8,2 × 10−5 m3 atm K−1 mol−1. T(K) = T(°C) + 273 Massas molares (g/mol): H = 1; C = 12. |
Gabarito:
Resolução:
a) O gasoduto é o cátodo. A proteção catódica consiste em utilizar um metal que oxide no lugar do metal que se deseja proteger. Em células eletroquímicas, a reação de oxidação ocorre no ânodo. Portanto, o metal utilizado para proteger o gasoduto é o ânodo e o gasoduto é o cátodo.
b) Como dito no item A, o metal a ser utilizado para proteger o gasoduto deve oxidar no seu lugar. Portanto, ele deve ter maior potencial de oxidação (ou menor potencial de redução) do que o metal que constitui o gasoduto. O enunciado da questão diz que o principal componente do gasoduto é o aço, uma liga majoritariamente composta por ferro. Dos metais apresentados na tabela, o único que possui potencial de redução menor do que o ferro é o zinco.
Em uma célula eletroquímica, cátodo é o polo positivo e o ânodo é o polo negativo. O zinco é o ânodo da célula em questão e, portanto, o polo negativo.
c)
• Cálculo da quantidade de matéria total da mistura:
• Cálculo da quantidade de matéria do gás etano.
Dessa quantidade de matéria, 4,1% corresponde ao gás etano. Essa quantidade pode ser calculada pela proporção
| 4065 mol mistura | __________ | netano |
| 100 mol mistura | __________ | 4,1 mol etano |
• Cálculo da massa correspondente à 166,67 mol de etano.
A massa de 1mol de etano é 30g. Portanto, a massa de 166,67 mol de etano pode ser calculada a partir da proporção
| 1 mol etano | __________ | 30g |
| 166,67 mol etano | __________ | metano |