Questão 8
[IME- 2015/2016 - 2ª fase]
Em um reservatório de volume de 6,0 L, submetido a vácuo, introduz-se uma mistura física de 79,2 g de gelo seco, solidificado em pequenos pedaços, com 30 g de carvão mineral em pó, conforme a representação a seguir.
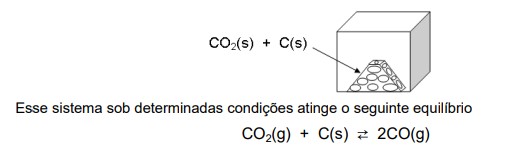
onde se observa que:
a fase gasosa tem comportamento de gás ideal;
o volume de carvão mineral final é desprezível;
a 1100 K a constante de equilíbrio da reação é Kp = 22;
a 1000 K a massa específica da fase gasosa no reservatório é igual a 14 g/L.
Com base nessas informações, calcule a constante de equilíbrio, Kp, da reação a 1000 K. Estabeleça se a reação entre o CO2(g) e o C(s) é exotérmica ou endotérmica, justificando sua resposta.
Gabarito:
Resolução:
Vamos calcular quanto de cada reagente temos:
| CO2 | + C |
2CO | |
| início (mol) | 1,8 | 2,5 | - |
| reage (mol) | -x | -x | 2x |
| equilíbrio (mol) | 1,8 - x | 2,5 - x | 2x |
| equilíbrio (massa) | 44(1,8 - x) | 12(2,5 - x) | 28(2x) |
Olhando para a fórmula da densidade temos a relação:
Sendo a massa da fase gasosa a soma da massa dos gases presentes (CO2 e CO), podemos dizer que:
Substituindo os valores da tabela:
Dessa forma temos:
| CO2 | + C |
2CO | |
| equilíbrio (mol) | 1,8 - 0,4 = 1,4 | 2,5 - 0,4 = 2,1 | 0,8 |
Podemos então calcular a concentração em mol por litro:
Sabendo as concentrações podemos calcular Kp:
A diminuição de temperatura (de 1100K para 1000K) também diminuiu a constante, o que implica que a reação foi desfavorecida, portanto a reação é endotérmica.