Questão 1
(IME - 2017/2018 - 2ª FASE ) Sabendo-se que e
são, respectivamente, isóbaro e isótono de um nuclídeo X determine para o íon hipotético X-1
a) a configuração eletrônica;
b) a camada de valência;
c) todos os números quânticos do elétron mais energético.
Gabarito:
Resolução:
a) Se Ti e X são isóbaros, isso implica que ambos possuem a mesma massa. Sendo assim, a massa de X também será 48.
Se V e X são isótonos, isso implica que ambos possuem o mesmo número de nêutrons. Como V tem 28 nêutrons (51-23=28), essa também será a quantidade de nêutrons de X.
Sabendo a massa e o número de nêutrons de X é possível saber seu número de prótons, já a massa é a soma do número de prótons e nêutrons:
Portanto, X tem 20 prótons.
Se o átomo é neutro, o número de prótons e elétrons é igual, e se X está com uma carga -1, isso implica que possui um elétron a mais em comparação com o átomo neutro, ou seja, 21 elétrons.
A distribuição eletrônica dos 21 elétrons é:
1s2 2s2 2p6 3s2 3p6 4s2 3d1
b) A camada de valência é o último nível a ser ocupado, que no caso do X-1, é a camada 4.
c) O elétron mais energético é o último da distribuição eletrônica, portanto, é 3d1. Esse elétron pode ser representado no diagrama de caixinhas como:
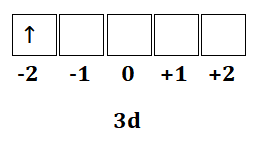
O conjunto de números quânticos será:
número quântico principal (nível) ⇒ 3
número quântico secundário (subnível) ⇒ 2
número quântico magnético ⇒ -2
número de spin ⇒ -1/2