Questão 6
(IME - 2017/2018 - 2ª FASE ) Em um vaso fechado, ocorreu a reação de 13,1 gramas de Xe(g) com excesso de F2(g) cuja pressão parcial é de 2,4 atm e a pressão total de 6 atm. Tal reação formou exclusivamente o composto apolar A, que possui 14 pares de elétrons não ligantes. Em seguida, foram adicionados 19,5 g de platina na forma sólida, que reagiram exclusivamente com o composto A para formar um produto X recuperando o gás nobre.
Considerando comportamento de gás ideal e sabendo que as reações ocorreram à temperatura de 400ºC determine:
a) a massa de flúor que não reagiu;
b) a estrutura de Lewis do composto A; e
c) a massa do produto X obtido.
Gabarito:
Resolução:
Segundo o enunciado, a reação de Xe com F2 levou a formação de um composto apolar com 14 pares de elétrons não ligantes, portanto, o composto formado foi XeF4. Essa reação pode ser representada por:
Xe(g) + 2 F2(g) → XeF4(g)
a) Para saber quanto de flúor não reagiu, é preciso saber quanto de Xe reagiu. Para isso, basta calcular a quantidade de matéria de Xe que reagiu, sabendo que a massa molar do Xe é 131g/mol:
1 mol de Xe ---------- 131 g
x ------------------------ 13,1 g
x = 0,1 mol de Xe
A pressão final total é igual soma da pressão de XeF4 mais a parcela que não reagiu de F2, sendo que a pressão total é 6 atm e a parcial de F2 é 2,4 atm. Com esses dados é possível calcular a pressão parcial de XeF4
A massa de flúor que não reagiu será:
A massa de 2,53g corresponde à massa que não reagiu de F2.
b) A estrutura de Lewis do XeF4 é:
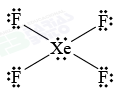
c) O produto X é obtido a partir da reação da Pt com XeF4, que pode ser representada pela equação:
XeF4(g) + Pt(s) → PtF4(s) + Xe(g)
Como foram adicionados 19,5 g de Pt que possui massa molar 195 g/mol, a quantidade de matéria adicionada foi de:
1 mol de Pt --------- 195 g
x ------------------------ 19,5 g
x = 0,1 mol de Pt
Segunfo a proporção estequiométrica da reação 1 mol de Pt forma 1 mol de PtF4, então 0,1 mol de Pt irá formar 0,1 mol de PtF4. Como a questão pergunta a massa de PtF4 é preciso converter sabendo que a massa molar é 271 g/mol:
1 mol de PtF4 --------- 271 g
0,1 mol de PtF4 ------ y
y = 27,1 g de PtF4
A massa obtida do produto X (PtF4) é 27,1 g.