Questão 100
(ITA - 2003)
Considere o elemento galvânico mostrado na figura a seguir. O semi-elemento A contém uma solução aquosa, isenta de oxigênio, 0,3 mol.L-1 em Fe2+ e 0,2 mol.L-1 em Fe3+. O semi-elemento B contém uma solução aquosa, também isenta de oxigênio, 0,2 mol.L-1 em Fe2+ e 0,3 mol.L-1 em Fe3+. M é um condutor metálico (platina). A temperatura do elemento galvânico é mantida constante num valor igual a 25°C.
A partir do instante em que a chave "S" é fechada, considere as seguintes afirmações:
I. O sentido convencional de corrente elétrica ocorre do semielemento B para o semielemento A.
II. Quando a corrente elétrica for igual a zero, a relação de concentrações [Fe3+(aq)] / [Fe2+(aq)] tem o mesmo valor tanto no semielemento A como no semielemento B.
III. Quando a corrente elétrica for igual a zero, a concentração de Fe2+(aq) no semielemento A será menor do que 0,3 mol L-1.
IV. Enquanto o valor da corrente elétrica for diferente de zero, a diferença de potencial entre os dois semielementos será maior do que 0, 118 log (3/2).
V. Enquanto corrente elétrica fluir pelo circuito, a relação entre as concentrações [Fe3+(aq)] / [Fe2+(aq)] permanece constante nos dois semielementos.
Das afirmações feitas, estão CORRETAS
Gabarito:
apenas I, II e III.
Resolução:
Vamos redesenhar a pilha com as concentrações em cada um delas:
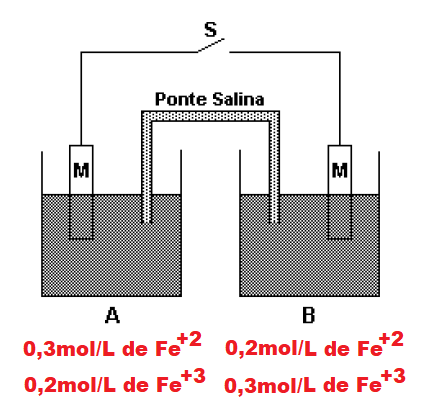
Nessa pilha o fluxo de elétrons vai ser em busca de igualar a concentração nos dois eletrodos.
Durante a descarga da pilha, no eletrodo A, a [Fe2+] diminuirá e a [Fe3+] aumentará A semirreação de oxidação que ocorre no ânodo, o pólo negativo, é:
Fe2+(aq) → Fe3+(aq) + e–
Durante a descarga da pilha, no eletrodo B, a [Fe2+] aumentará e a [Fe3+] diminuirá. A semirreação de redução que ocorre no cátodo, pólo positivo, é:
Fe3+(aq) + e– → Fe2+(aq)
I) CORRETA. O fluxo de elétrons, pelo circuito externo, será do eletrodo A para o eletrodo B e, com isso, a corrente elétrica convencional terá sentido oposto, indo do semielemento B para o semielemento A.
II) CORRETA. Quando a corrente for zero, não há fluxo de elétrons mais. Então a relação de concentrações [Fe3+(aq)] e [Fe2+(aq)] vai ser igual nos dois eletrodos.
III) CORRETA. Na descarga da pilha, a concentração, em mol/L, de Fe2+ está diminuindo. Logo, quando a pilha se esgotar, a [Fe2+] será menor do que 0,3molL–1.
IV) INCORRETA. Pela equação de Nernst podemos calcular o ∆ε do início da reação:
(no início)
À medida que a pilha descarrega, o ∆ε diminui.
V) INCORRETA. A concentração varia até chegar em uma constante.