Questão 26
(ITA - 2007 - 2 fase - Questão 26)
A tabela abaixo apresenta os valores das temperaturas de fusão (Tf) e de ebulição (Te) de halogênios e haletos de hidrogênio.
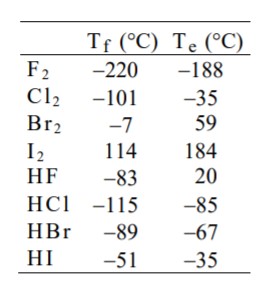
(a) Justifique a escala crescente das temperaturas Tf e Te do F2 ao I2.
(b) Justifique a escala decrescente das temperaturas Tf e Te do HF ao HCℓ.
(c) Justifique a escala crescente das temperaturas Tf e Te do HCℓ ao HI .
Gabarito:
Resolução:
a)
Quanto maior for um átomo, mais polarizável ele é, o que possibilita a existência de um dipolo elétrico maior e faz com que as interações intermoleculares sejam mais fortes. Por esse motivo as interações intermoleculares do I2 são as mais intensas entre as substâncias em questão e as do F2 são as menos intensas. Quanto maior for a intensidade das interações intermoleculares, maiores são as temperaturas de fusão e ebulição.
b)
As interações intermoleculares do HF são ligações de hidrogênio, que são interações mais fortes do que as dipolo-dipolo entre as moléculas de HCl. Como as interações intermoleculares do HF são mais fortes do que as do HCl, as temperaturas de fusão e ebulição do HF são maiores.
c)
Novamente, quanto maior o raio de um átomo, mais polarizável ele é e mais intensas são as forças moleculares. Quanto mais fortes forem as interações intermoleculares, maiores são as temperaturas de ebulição.