Questão 56
(ITA - 2021- 1a Fase)
Considerando substâncias comparadas nas mesmas condições de pressão e temperatura, assinale a opção que apresenta a afirmação ERRADA sobre interações intermoleculares na fase líquida.
Cis-1,2-dicloroeteno tem maior tensão superficial que trans-1,2-dicloroeteno.
Bezeno tem maior tensão superficial que hexano.
Propanona tem maior viscosidade que butano.
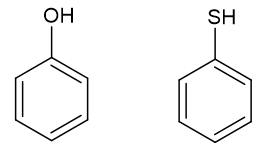
Tiofenol tem maior viscosidade que fenol.
A capilaridade da água em um tubo de vidro é maior que a do etanol.
Gabarito:
Tiofenol tem maior viscosidade que fenol.
Resolução:
Analisando cada uma das alternativas.
[A] Verdadeira. A molécula cis tem interação intermolecular mais forte, já que o seu momento de dipolo é maior. A molécula cis é uma molécula polar, podendo interagir por interações dipolo-dipolo. A molécula trans é apolar, tendo uma interação dipolo-induzido.
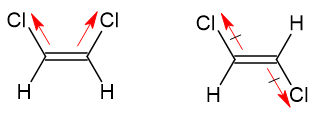
Se a força da interação intermolecular é maior, a tensão superficial também. Então, a molécula cis terá maior tensão superficial.
[B] Verdadeira. O benzeno empacota melhor, por isso tem maior tensão superficial.
[C] Verdadeira. A propanona é uma molécula com função orgânica cetona. Por isso, ela será polar e pode interagir por dipolo-dipolo. O butano é uma molécula apolar, tendo uma interação mais fraca que a propanona. A interação intermolecular da propanona é maior, por isso sua viscosidade vai ser maior.
[D] Falso. A viscosidade do fenol é maior porque a interação intermolecular é mais forte. A molécula do fenol faz interações por ligações de hidrogênio (apresenta hidrogênio ligado ao oxigênio), enquanto que o tiofenol não pode fazer esse tipo de interação (apresenta hidrogênio ligado ao enxofre).
[E] Verdadeiro. A interação da água é maior porque não apresenta parte apolar em sua estrutura, enquanto que o etanol apresenta uma cadeia carbônica de 2 carbonos. Como a interação intermolecular da água é mais forte, ela terá maior viscosidade.