Questão 69
(ITA - 2021- 1a Fase)
Considerando os átomos de F mais afastados um do outro, assinale a opção que apresenta as moléculas na ordem de maior para menor ângulo da ligação F - Y - F (Y = S, Cl ou Xe).
Dados:
números atômicos (Z): F = 9 ; S = 16 ; Cl = 17 ; Xe = 54.
ClF3, SF4, XeF+3
ClF3, XeF+3, SF4
SF4, ClF3, XeF+3
SF4, XeF+3, ClF3
XeF+3, SF4, ClF3
Gabarito:
ClF3, SF4, XeF+3
Resolução:
Essas são as estruturas do ClF3, SF4, XeF3+ na ordem descrescente dos ângulos de ligação F-Y-F.
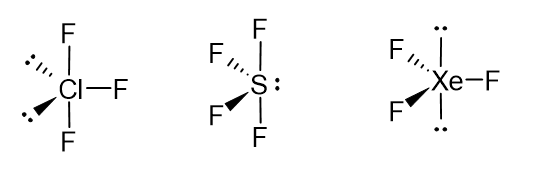
A questão pede os ângulos de ligação de F-Y-F entre os átomos de flúor mais afastados. O ângulo de ligação no XeF3+ é 120º. Os ângulos de ligação no SF4 e no ClF3 são maiores do que 180º porque há uma força de repulsão entre o(s) par(es) de elétron(s) e os átomos de flúor. Como o ClF3 tem dois pares de elétrons e o SF4 só tem um, a repulsão entre os pares de elétrons é maior no ClF3, fazendo com que o ângulo de ligação também seja maior.