Questão 10515
(ITA - 2000)
A figura abaixo mostra como a entalpia dos reagentes e dos produtos de uma reação química do tipo A (g) + B (g) →C (g) varia com a temperatura. Levando em consideração as informações fornecidas nessa figura e sabendo que a variação de entalpia (ΔH) é igual ao calor trocado pelo sistema à pressão constante, é errado afirmar que:
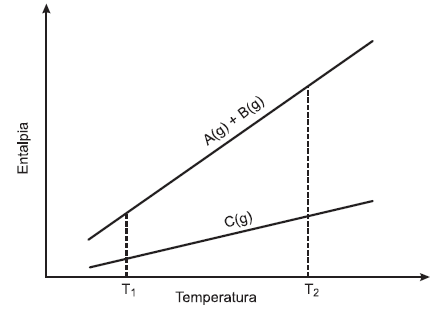
na temperatura T1, a reação ocorre com liberação de calor.
na temperatura T1, a capacidade calorífica dos reagentes é maior que a dos produtos.
no intervalo de temperatura compreendido entre T1 e T2, a reação ocorre com absorção de calor (ΔH> zero).
o ΔH, em módulo, da reação aumenta com o aumento de temperatura.
tanto a capacidade calorífica dos reagentes como a dos produtos aumentam com o aumento da temperatura.
Gabarito:
no intervalo de temperatura compreendido entre T1 e T2, a reação ocorre com absorção de calor (ΔH> zero).
Resolução:
Analisando as alternativas:
A) na temperatura T1, a reação ocorre com liberação de calor.
INCORRETA. Veja que a entalpia dos reagentes, em qualquer temperatura, é maior que a entalpia dos produtos. Isso quer dizer que temos uma reação exotérmica, com liberação de energia em forma de calor.
B) na temperatura T1, a capacidade calorífica dos reagentes é maior que a dos produtos.
CORRETA. A capacidade calorífica será a razão entre a quantidade de calor de uma substância e sua variação de temperatura:
A temperatura constante, o calor é igual a variação de entalpia da substância:
Logo, quanto maior a entalpia, maior será sua capacidade calorífica.
C) no intervalo de temperatura compreendido entre T1 e T2, a reação ocorre com absorção de calor (ΔH> zero).
INCORRETO. Essa é uma reação exotérmica, teremos, então, a liberação de calor.
D) o ΔH, em módulo, da reação aumenta com o aumento de temperatura.
CORRETO. Pelo gráfico, observamos que, com o aumento da temperatura, o ΔH da reação aumenta.
E) tanto a capacidade calorífica dos reagentes como a dos produtos aumentam com o aumento da temperatura.
CORRETO. Como vimos na letra B), a capacidade calorífica é diretamente proporcional a variação de entalpia.