FUVEST 2007
Questão 51137
UNICAMP
(UNICAMP - 2007) As frutas são produtos agrícolas de grande importância comercial e nutricional. Em sua comercialização, podem ocorrer problemas de transporte, de conservação e de consumo. Para evitar danos de armazenamento e transporte, elas são colhidas ainda verdes, sendo, neste estágio, impróprias para o consumo. Por dádiva da natureza, algumas dessas frutas amadurecem mesmo após a colheita. Esse processo pode ser controlado artificialmente. Essas frutas a que se faz alusão, quando colocadas em um recinto fechado, e tratadas com etileno ou acetileno gasosos, têm seu processo de amadurecimento acelerado. Esse fato é conhecido desde 1940, quando se descobriu que a liberação de gás etileno pelas frutas cítricas é essencial para o seu amadurecimento.
a) Em vista dessas informações, que procedimento muito simples você poderia utilizar em sua casa para acelerar o amadurecimento de frutas cítricas? Descreva resumidamente o procedimento.
b) Dispondo-se de carbeto de cálcio, é possível utilizá-lo para acelerar o amadurecimento de frutas. Justifique esta afirmação com uma equação química.
c) Os dois gases apresentados no texto, sob mesma condição de temperatura e pressão, têm densidades muito próximas, mas um deles é mais denso. Qual é o mais denso? Justifique sua resposta.
Questão 51138
UNICAMP
(UNICAMP - 2007) A verificação de uma das propriedades do solo consiste em suspender uma amostra de 5,0 cm3 do solo em um volume de 100 mL de uma solução aquosa de acetato de cálcio por certo tempo e sob agitação vigorosa. Depois da decantação, o sobrenadante é separado e titulado com uma solução aquosa de hidróxido de sódio de concentração conhecida.
a) Segundo esse procedimento, qual propriedade do solo pode-se supor que se pretende determinar? Justifique sua resposta.
b) No procedimento de titulação acima mencionado, o que deve ser feito para que o ponto final possa ser observado?
c) Escreva a equação química da reação envolvida nessa titulação
Questão 51139
UNICAMP
(UNICAMP - 2007) Um artigo publicado no The Agronomy Journal de 2006 trata de um estudo relacionado à fixação de nitrogênio por uma planta forrageira que se desenvolve bem em um solo ácido. Essa planta tem o crescimento limitado pela baixa fixação de nitrogênio. O objetivo central do trabalho era verificar como uma cultura de alfafa, cultivada junto à forrageira citada, poderia melhorar o crescimento da forrageira, aumentando a fixação de nitrogênio. Relata o artigo que o terreno a ser adubado foi subdividido em cinco partes. Cada parte foi adubada com as seguintes quantidades fixas de nitrato de amônio, a cada vez: 0; 28; 56; 84; 112 kg/ha. As adubações foram repetidas por 15 vezes em períodos regulares, iniciando-se no começo de 1994 e encerrando-se no final de 1996. Para monitorar a fixação de nitrogênio, os pesquisadores adicionaram uma pequeníssima quantidade conhecida de nitrato de amônio marcado () ao nitrato de amônio comercial a ser aplicado na plantação.
a) Do ponto de vista da representação química, o que significa o sobrescrito 15 junto ao símbolo N?
b) Suponha duas amostras de mesma massa, uma de e a outra de
. A quantidade de nitrogênio (em mol) na amostra de
é maior, igual ou menor do que na amostra de
? Justifique sua resposta.
c) Considere que na aplicação regular de 28 kg/ha não sobrou nem faltou adubo para as plantas. Determine, em mol/ha, que quantidade desse adubo foi aplicada em excesso na parte que recebeu 112 kg/ha, ao final do primeiro ano de estudo.
Questão 51141
UNICAMP
(UNICAMP - 2007) A aplicação de insumos químicos na atividade agrícola pode representar uma fonte de problemas ambientais e econômicos, se não for feita corretamente. Em um estudo realizado para monitorar as perdas de um agrotóxico em uma plantação de tomates, uma solução aquosa de um sal duplo de cobre foi aplicada por pulverização. As perdas para o solo e para o ambiente foram determinadas por análise química do cobre.
a) A quantidade total (em gramas) de um agrotóxico (Q) pulverizado numa área pré-determinada do tomatal pode ser obtida conhecendo-se algumas grandezas. Escreva uma equação matemática que permita calcular Q, escolhendo entre as grandezas: t (tempo de pulverização em segundos); T (temperatura em kelvin); V (vazão de solução pulverizada em L s-1); F (massa de solução pulverizada em kg s-1); C (concentração do agrotóxico no líquido pulverizado em mol L-1); P (porcentagem em massa de agrotóxico por massa de líquido); M (massa molar do agrotóxico).
b) Sabendo-se que o agrotóxico utilizado é um hidroxi-cloreto de cobre, e que a sua massa molar é de 213,4 g mol-1, escreva a sua fórmula.
c) De acordo com a fórmula do agrotóxico, em que estado de oxidação encontra-se o cobre? Justifique sua resposta.
Questão 51142
UNICAMP
(UNICAMP - 2007) Quando se utiliza um biossistema integrado numa propriedade agrícola, a biodigestão é um dos processos essenciais desse conjunto. O biodigestor consiste de um tanque, protegido do contato com o ar atmosférico, onde a matéria orgânica de efluentes, principalmente fezes animais e humanas, é metabolizada por bactérias. Um dos subprodutos obtidos nesse processo é o gás metano, que pode ser utilizado na obtenção de energia em queimadores. A parte sólida e líquida que sobra é transformada em fertilizante. Dessa forma, faz-se o devido tratamento dos efluentes e ainda se obtêm subprodutos com valor agregado.
a) Sabe-se que a entalpia molar de combustão do metano é de -803 kJ/mol; que a entalpia molar de formação desse mesmo gás é de -75 kJ/mol; que a entalpia molar de formação do CO2 é de -394 kJ/mol. A partir dessas informações, calcule a entalpia molar de formação da água nessas mesmas condições.
No aparelho digestório de um ruminante ocorre um processo de fermentação de hexoses, semelhante ao que ocorre nos biodigestores. A equação abaixo tem sido utilizada para representar essa fermentação:
b) Considere a seguinte afirmação: “o processo de fermentação digestiva de ruminantes contribui para o aquecimento global”. Você concorda? Responda SIM ou NÃO e explique sua resposta.
c) Qual seria o número de moles de gás metano produzido na fermentação de 5,8 quilogramas de hexose ingeridos por um ruminante?
Questão 51143
UNICAMP
(UNICAMP - 2007) O boro é um micronutriente para plantas com importante papel no processo de germinação e na formação de frutos, de grãos e de sementes. A solubilidade dos sais de boro em água constitui um problema para a correção da deficiência desse elemento, que é facilmente “arrastado” pela chuva. Esse problema pode ser contornado pelo uso de materiais que adsorvam os sais de boro, liberando-os lentamente para a umidade do solo. O gráfico abaixo mostra a quantidade de boro adsorvido (Y/m) por alguns materiais em função da concentração do boro em solução
aquosa
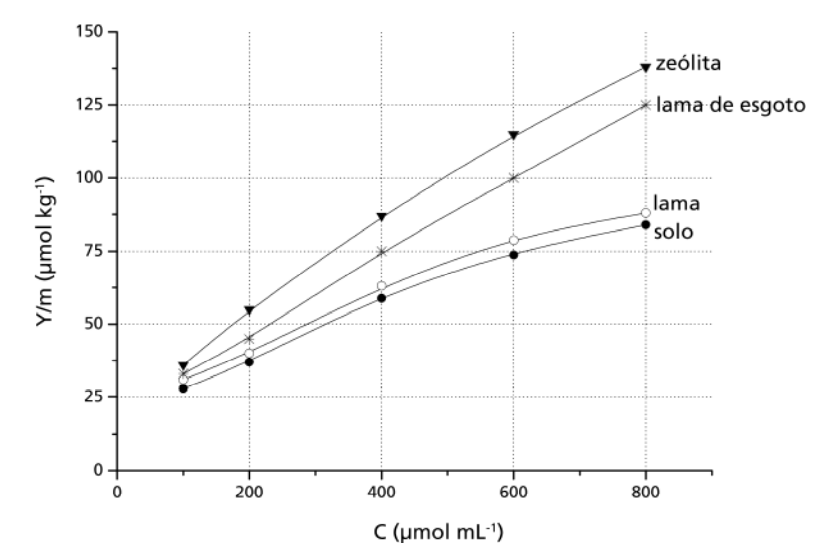
De acordo com o gráfico:
a) Dos materiais em questão, qual é o mais eficiente para a retenção do boro? Justifique sua resposta.
b) Para uma concentração de boro de 600 µmol mL-1, quanto o material do item a adsorve a mais que o solo em µmol de boro por tonelada?
c) Entre as concentrações de 300 e 600 µmol mL-1, as adsorções podem ser descritas, aproximadamente, por retas. Levando isso em conta, escreva, para o caso da lama de esgoto, a equação da reta que correlaciona Y/m com C.
Ver questão
Questão 51144
UNICAMP
(UNICAMP - 2007) No mundo do agronegócio, a criação de camarões, no interior do nordeste brasileiro, usando águas residuais do processo de dessalinização de águas salobras, tem se mostrado uma alternativa de grande alcance social. A dessanilização consiste num método chamado de osmose inversa, em que a água a ser purificada é pressionada sobre uma membrana semipermeável, a uma pressão superior à pressão osmótica da solução, forçando a passagem de água pura para o outro lado da membrana. Enquanto a água dessalinizada é destinada ao consumo de populações humanas, a água residual (25 % do volume inicial), em que os sais estão concentrados, é usada para a criação de camarões.
a) Supondo que uma água salobra que contém inicialmente 10.000 mg de sais por litros sofre a dessalinização conforme descreve o texto, calcule a concentração de sais na água residual formada em mg L-1.
b) Calcule a pressão mínima que deve ser aplicada, num sistema de osmose inversa, para que o processo referente ao item a acima tenha início. A pressão osmótica de uma solução pode ser calculada por uma equação semelhante à dos gases ideais, onde n é o número de moles de partículas por litro de solução. Para fins de cálculo, suponha que todo o sal dissolvido na água salobra seja cloreto de sódio e que a temperatura da água seja de 27 ºC. Dado: constante dos gases, R = 8.314 Pa L K-1 mol-1.
c) Supondo que toda a quantidade (em mol) de cloreto de sódio do item b tenha sido substituída por uma quantidade igual (em mol) de sulfato de sódio, pergunta-se: a pressão a ser aplicada na osmose à nova solução seria maior, menor ou igual à do caso anterior? Justifique sua resposta
Questão 51145
UNICAMP
(UNICAMP - 2007) Uma hexose, essencial para o organismo humano, pode ser obtida do amido, presente no arroz, na batata, no milho, no trigo, na mandioca, ou da sacarose proveniente da cana-de-açúcar. A sua fórmula estrutural pode ser representada como uma cadeia linear de carbonos, apresentando uma função aldeído no primeiro carbono. Os demais carbonos apresentam, todos, uma função álcool, sendo quatro representadas de um mesmo lado da cadeia e uma quinta, ligada ao terceiro carbono, do outro lado. Essa mesma molécula (hexose) também pode ser representada na forma de um anel de seis membros, com cinco átomos de carbono e um de oxigênio, já que o oxigênio do aldeído acaba se ligando ao quinto carbono.
a) Desenhe a fórmula estrutural linear da hexose de modo que a cadeia carbônica fique na posição vertical e a maioria das funções álcool fique no lado direito.
b) A partir das informações do texto, desenhe a estrutura cíclica dessa molécula de hexose.
Questão 51175
UNICAMP
(UNICAMP - 2007) "Pão por quilo divide opiniões em Campinas” (Correio Popular, 21/10/2006).
Uma padaria de Campinas vendia pães por unidade, a um preço de R$ 0,20 por pãozinho de 50 g. Atualmente, a mesma padaria vende o pão por peso, cobrando R$ 4,50 por quilograma do produto.
a) Qual foi a variação percentual do preço do pãozinho provocada pela mudança de critério para o cálculo do preço?
b) Um consumidor comprou 14 pãezinhos de 50 g, pagando por peso, ao preço atual. Sabendo que os pãezinhos realmente tinham o peso previsto, calcule quantos reais o cliente gastou nessa compra.
Questão 51176
UNICAMP
(UNICAMP - 2007) A fi gura abaixo mostra um fragmento de mapa, em que se vê o trecho reto da estrada que liga as cidades de Paraguaçu e Piripiri. Os números apresentados no mapa representam as distâncias, em quilômetros, entre cada cidade e o ponto de início da estrada (que não aparece na fi gura). Os traços perpendiculares à estrada estão uniformemente espaçados de 1 cm.
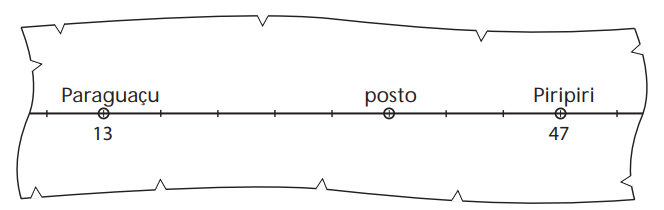
a) Para representar a escala de um mapa, usamos a notação 1: X, onde X é a distância real correspondente à distância de 1 unidade do mapa. Usando essa notação, indique a escala do mapa dado acima.
b) Repare que há um posto exatamente sobre um traço perpendicular à estrada. Em que quilômetro (medido a partir do ponto de início da estrada) encontra-se tal posto?
c) Imagine que você tenha que reproduzir o mapa dado usando a escala 1: 500000. Se você fizer a figura em uma folha de papel, qual será a distância, em centímetros, entre as cidades de Paraguaçu e Piripiri?
Ver questão