FUVEST 2015
Questão 36110
UNESP
(UNESP - 2015 - 2 FASE) A figura representa duas raias de uma pista de atletismo plana. Fábio (F) e André (A) vão apostar uma corrida nessa pista, cada um correndo em uma das raias. Fábio largará à distância da linha de partida para que seu percurso total, de F até a chegada em C', tenha o mesmo comprimento do que o percurso total de André, que irá de A até D'.
Considere os dados:
- ABCD e A 'B 'C'D' são retângulos.
- B ', A ' e E estão alinhados.
- C, D e E estão alinhados.
- e
são arcos de circunferência de centro E.
Sabendo que ,
,
,
e
, calcule o comprimento da pista de A até D' e, em seguida, calcule a distância
. Adote nos cálculos finais
Questão 36286
FUVEST
(FUVEST 2015 - 2ª fase) O metabissulfito de potássio (K2S2O5) e o dióxido de enxofre (SO2) são amplamente utilizados na conservação de alimentos como sucos de frutas, retardando a deterioração provocada por bactérias, fungos e leveduras. Ao ser dissolvido em soluções aquosas ácidas ou básicas, o metabissulfito pode se transformar nas espécies químicas SO2, HSO3- ou SO32- , dependendo do pH da solução, como é mostrado no gráfico.
A equação a seguir representa a formação dos íons HSO3- em solução aquosa.
a) Escreva as equações químicas balanceadas que representam a formação das espécies químicas SO2 (aq) e SO32-(aq) a partir dos íons S2O52-(aq).
b) Reações indesejáveis no organismo podem ocorrer quando a ingestão de íons S2O52- , HSO3- ou SO32- ultrapassa um valor conhecido como IDA (ingestão diária aceitável, expressa em quantidade de SO2/dia/massa corpórea), que, neste caso, é igual a 1,1 x 10-5 mol de SO2 por dia para cada quilograma de massa corpórea. Uma pessoa que pesa 50 kg tomou, em um dia, 200 mL de uma água de coco industrializada que continha 64 mg/L de SO2. Essa pessoa ultrapassou o valor da IDA? Explique, mostrando os cálculos.
Questão 36287
FUVEST
(FUVEST 2015 - 2ª fase) O hidrogênio tem sido apontado como possível fonte de energia do futuro. Algumas montadoras de automóveis estão construindo carros experimentais que podem funcionar utilizando gasolina ou hidrogênio líquido como combustível. Considere a tabela a seguir, contendo dados obtidos nas mesmas condições, sobre a energia específica (quantidade de energia liberada pela combustão completa de 1 g de combustível) e o conteúdo de energia por volume (quantidade de energia liberada pela combustão completa de 1 L de combustível), para cada um desses combustíveis:
a) Com base nos dados da tabela, calcule a razão entre as densidades da gasolina líquida e do hidrogênio líquido (dgasolina(l)/ dhidrogênio(l)). Mostre os cálculos.
b) Explique por que, embora a energia específica do hidrogênio líquido seja maior do que a da gasolina líquida, o conteúdo de energia por volume do hidrogênio líquido é menor do que o da gasolina líquida.
Ver questãoQuestão 36288
FUVEST
(FUVEST 2015 - 2ª fase) A preparação de um biodiesel, em uma aula experimental, foi feita utilizando‐se etanol, KOH e óleo de soja, que é constituído principalmente por triglicerídeos. A reação que ocorre nessa preparação de biodiesel é chamada transesterificação, em que um éster reage com um álcool, obtendo‐se um outro éster. Na reação feita nessa aula, o KOH foi utilizado como catalisador. O procedimento foi o seguinte:
1ª etapa: Adicionou‐se 1,5 g de KOH a 35 mL de etanol, agitando‐se continuamente a mistura.
2ª etapa: Em um erlenmeyer, foram colocados 100 mL de óleo de soja, aquecendo‐se em banho‐maria, a uma temperatura de 45ºC. Adicionou‐se a esse óleo de soja a solução de catalisador, agitando‐se por mais 20 minutos.
3ª etapa: Transferiu‐se a mistura formada para um funil de separação, e esperou‐se a separação das fases, conforme representado na figura ao lado
a) Toda a quantidade de KOH, empregada no procedimento descrito, se dissolveu no volume de etanol empregado na primeira etapa? Explique, mostrando os cálculos.
b) Considere que a fórmula estrutural do triglicerídeo contido no óleo de soja é a mostrada ao lado. Escreva, no espaço indicado na página de respostas, a fórmula estrutural do biodiesel formado.
,
c) Se, na primeira etapa desse procedimento, a solução de KOH em etanol fosse substituída por um excesso de solução de KOH em água, que produtos se formariam? Responda, completando o esquema da página de respostas com as fórmulas estruturais dos dois compostos que se formariam e balanceando a equação química.
Questão 36289
FUVEST
(FUVEST 2015 - 2ª fase) Compostos com um grupo NO2 ligado a um anel aromático podem ser reduzidos, sendo o grupo NO2 transformado em NH2, como representado ao lado.
Compostos alifáticos ou aromáticos com grupo NH2, por sua vez, podem ser transformados em amidas ao reagirem com anidrido acético. Essa transformação é chamada de acetilação do grupo amino, como exemplificado ao lado.
Essas transformações são utilizadas para a produção industrial do paracetamol, que é um fármaco empregado como analgésico e antitérmico.
a) Qual é o reagente de partida que, após passar por redução e em seguida por acetilação, resulta no paracetamol? Escreva a fórmula estrutural desse reagente, no quadro da página de respostas.
O fenol (C6H5OH) também pode reagir com anidrido acético. Nessa transformação, forma‐se acetato de fenila.
b) Na etapa de acetilação do processo industrial de produção do paracetamol, formam‐se, também, ácido acético e um subproduto diacetilado (mas monoacetilado no nitrogênio). Complete o esquema da página de respostas, de modo a representar a equação química balanceada de formação do subproduto citado.
Ver questãoQuestão 36290
FUVEST
(FUVEST - 2015)
A figura ao lado ilustra as estabilidades relativas das espécies que apresentam estado de oxidação +2 e +4 dos elementos da mesma família: carbono, silício, germânio, estanho e chumbo.
As estabilidades relativas podem ser interpretadas pela comparação entre potenciais padrão de redução das espécies +4 formando as espécies +2, como representado a seguir para os elementos chumbo (Pb), germânio (Ge) e estanho (Sn):
Os potenciais padrão de redução dessas três semirreações, E1º , E2º e E3º , foram determinados experimentalmente, obtendo‐se os valores -0,12 V, -0,094 V e 1,5 V, não necessariamente nessa ordem. Sabe‐se que, quanto maior o valor do potencial padrão de redução, maior o caráter oxidante da espécie química.
a) Considerando as informações da figura, atribua, na tabela da página de respostas, os valores experimentais aos potenciais padrão de redução E1º , E2º e E3º.
b) O elemento carbono pode formar óxidos, nos quais a proporção entre carbono e oxigênio está relacionada ao estado de oxidação do carbono. Comparando os óxidos CO e CO2, qual seria o mais estável? Explique, com base na figura apresentada acima.
Ver questãoQuestão 36291
FUVEST
(FUVEST 2015 - 2ª fase) O glicerol pode ser polimerizado em uma reação de condensação catalisada por ácido sulfúrico, com eliminação de moléculas de água, conforme se representa a seguir:
a) Considerando a estrutura do monômero, pode‐se prever que o polímero deverá ser formado por cadeias ramificadas. Desenhe a fórmula estrutural de um segmento do polímero, mostrando quatro moléculas do monômero ligadas e formando uma cadeia ramificada.
Para investigar a influência da concentração do catalisador sobre o grau de polimerização do glicerol (isto é, a porcentagem de moléculas de glicerol que reagiram), foram efetuados dois ensaios:
Ao final desses ensaios, os polímeros 1 e 2 foram analisados separadamente. Amostras de cada um deles foram misturadas com diferentes solventes, observando‐se em que extensão ocorria a dissolução parcial de cada amostra. A tabela a seguir mostra os resultados dessas análises:
b) Qual dos polímeros formados deve apresentar menor grau de polimerização? Explique sua resposta, fazendo referência à solubilidade das amostras em etanol.
Ver questãoQuestão 36310
FUVEST
(FUVEST - 2015 - 2 FASE)
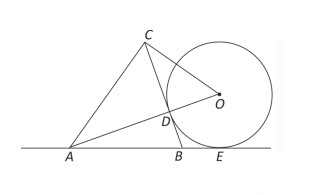
Na figura, na página de respostas, a circunferência de centro em 0 ܱ e raio r tangencia o lado do triângulo ABC no ponto D e tangencia a reta
no ponto E .Os pontos A,D e ܱ0 são colineares, AD = 2r e o ângulo
ܱé reto. Determine, em função de r,
a) a medida do lado do triângulo ABC;
b) a medida do segmento .
Questão 36311
FUVEST
(FUVEST - 2015 - 2 FASE)
Resolva as inequações:
a) x3 — x2 — 6x > 0;
b) log2 (x3-x2-6x) 2.
Questão 36312
FUVEST
(FUVEST - 2015 - 2 FASE)
No cubo ABCDEFGH, representado na figura, na página de respostas, cada aresta tem medida 1. Seja M um ponto na semirreta de origem A que passa por E. Denote por o ângulo
e por x a medida do segmento
.
a) Exprima cos em função de x
b) Para que valores de x o ângulo é obtuso?
c) Mostre que, se x = 4, então mede menos do que 45º.