ITA 2023
Questão 82197
ESPCEX
(EsPCEx - 2023)
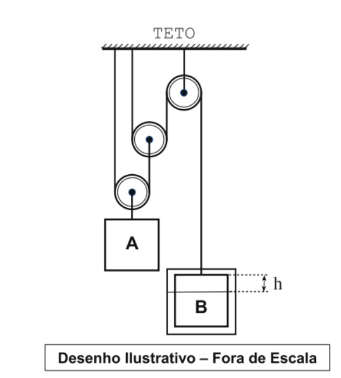
O desenho a seguir representa um sistema em equilíbrio estático, preso ao teto e composto por: polias e fios ideais de massas desprezíveis; pelos cubos A e B, feitos de mesma substância e com arestas iguais de comprimento L. O cubo B está parcialmente imerso em um líquido homogêneo dentro de um recipiente. Observa-se que uma parte da aresta do cubo B, de comprimento , é a altura da parte emersa do cubo. Podemos afirmar que a razão entre a densidade dos cubos e a densidade do líquido é:
Questão 82198
ESPCEX
(EsPCEx - 2023)
Uma máquina térmica opera segundo o ciclo de Carnot com um rendimento de 0,2. Se aumentarmos a temperatura da fonte quente em 25%, o novo rendimento dessa máquina térmica, segundo o ciclo de Carnot, será de:
Ver questãoQuestão 82199
ESPCEX
(EsPCEx - 2023)
Uma substância pura pode se apresentar em três estados de agregação: sólido, líquido e gasoso. Com relação as mudanças de fase a pressão constante de uma determinada substância pura, podemos afirmar que:
Ver questãoQuestão 82200
ESPCEX
(EsPCEx - 2023)
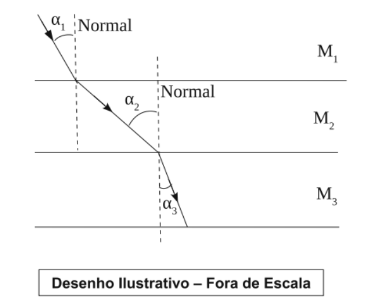
O desenho a seguir representa um raio de luz monocromática que atravessa três meios distintos e homogêneos M1, M2 e M3 cujos índices de refração são iguais a n1, n2 e n3, respectivamente. Os ângulos a1, a2 e a3 são formados entre o raio e a normal às respectivas superfícies planas e horizontais de separação entre os meios. Supondo que podemos afirmar que:
Questão 82201
ESPCEX
(EsPCEx - 2023)
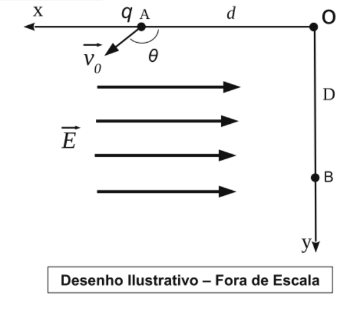
O desenho a seguir representa o espaço que foi mapeado com os eixos cartesianos xy com origem no ponto O. Na região, há um campo elétrico uniforme de sentido contrário à orientação do eixo x. Uma carga elétrica puntiforme positiva q, de massa m, é lançada do ponto A, do eixo x, com uma velocidade inicial
, na região em que o campo atua. Ela desloca-se sob ação exclusiva do campo elétrico até chocar-se em um anteparo, no ponto B do eixo y, conforme representado no desenho. Podemos afirmar que o módulo da carga elétrica q é dado por:
Dados: o ângulo entre e
vale
;
;
e
.
Questão 82202
ESPCEX
(EsPCEx - 2023)
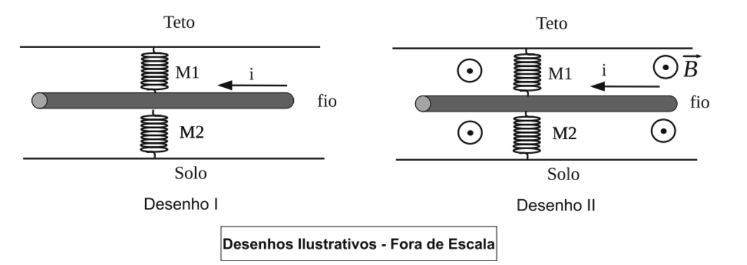
O Desenho I representa um fio condutor retilíneo homogêneo, horizontal e de comprimento L percorrido por uma corrente elétrica i . O centro de massa do fio está conectado a molas ideais e verticais M1 e M2. A mola M1 esta conectada ao teto, e M2, ao solo, conforme indicado no Desenho I. O sistema encontra-se em equilíbrio estático. As molas M1 e M2 estão, respectivamente, com um aumento e uma diminuição, de módulo igual a x0, em seu comprimento natural. Em seguida, todo o fio condutor fica imerso em um campo magnético uniforme de intensidade B, conforme representado no Desenho II. O sistema atinge um novo equilíbrio estático, com o fio na horizontal e M1 e M2 sofrendo, respectivamente, uma diminuição e um aumento, de módulo igual a x1, em seu comprimento natural. Podemos afirmar que x0, é igual a:
Dados: M1 e M2 têm constante elástica, respectivamente, igual a k1 e k2 ;  representa o vetor campo magnético
representa o vetor campo magnético que é perpendicular ao plano do papel e está saindo dele; e o fio condutor esta no plano do papel.
Questão 82203
ESPCEX
(EsPCEx - 2023)
Considere a seguinte descrição de um experimento de laboratório:
Materiais e reagentes
- duas porções de zinco em pó com massa de 0,3 g cada uma
- uma placa de zinco laminado com 0,3 g
- solução de ácido cloridrico concentrado (12,0 mol L-1)
- solução de ácido clorídrico diluido (0,05 mol L-1)
- 3 copos de béquer identificados pelas letras A,B e C
- cronômetro
Procedimento
Coloque 30,0 mL da solução de ácido clorídrico concentrado nos copos de béquer A e B, e coloque 30,0 mL da solução de ácido clorídrico diluido no copo de béquer C. Em seguida, coloque simultaneamente a placa de zinco no copo de béquer A e uma porção de 0,3 g de zinco em pó no copo de béquer B. Meça o tempo decorrido até o consumo total do zinco em cada copo de béquer. Posteriormente, coloque uma porção de 0,3 g de zinco em pó no copo de béquer C. Mega o tempo decorrido até o consumo total do zinco nesse copo de béquer. Observe o que ocorre e anote os dados. Considerando-se que os sistemas estavam inicialmente em iguais condições e que foi observada a ocorrência de reação nos três experimentos realizados nos copos de béquer, são feitas as seguintes afirmativas acerca do experimento e das reações ocorridas:
I- Em todos os copos de béquer ocorreu a formação de clorato de zinco e gás carbônico como produtos de reação.
II- Devido a maior superfície de contato do reagente metálico em pó em relação a lamina, a velocidade da reação observada no copo de béquer B sera maior do que no copo de béquer A.
III- As reações ocorridas nos experimentos podem ser classificadas como reações de oxidorredugao.
IV- Devido à maior concentragio da solução ácida 12,0 mol L-1 em relagdo a solução 0,05 mol L-1, a velocidade da reação observada no copo de béquer B será menor do que no copo de béquer C.
V- Segundo a teoria de Bronsted-Lowry, na reação entre o ácido clorídrico e a água, o íon cloreto é a base conjugada do ácido.
Das afirmativas feitas, estão corretas apenas
Ver questãoQuestão 82204
ESPCEX
(EsPCEx - 2023)
A alternativa que apresenta corretamente os conceitos químicos sobre as caracteristicas de substâncias simples e compostas e de elementos químicos é:
Ver questãoQuestão 82205
ESPCEX
(EsPCEx - 2023)
Algumas granadas incendiárias, como as do modelo AN-M14 TH3, possuem em sua composição alumínio metálico em pó e óxido de ferro Ill. Quando acionadas, elas produzem uma reação extremamente exotérmica, que pode atingir temperaturas da ordem de 3000 °C. Por essa característica, são utilizadas para destruir ou inutilizar equipamentos. A reação aluminotérmica que ocorre na granada é representada pela seguinte equação química:
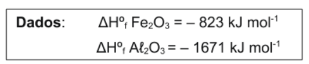
Considerando-se a reação de 352 g de óxido de ferro Ill com 135 g de alumínio, sob condições-padrão, são feitas as seguintes afirmativas:
I- Nessas condições, o reagente limitante é o alumínio metálico.
II - O número de oxidação do alumínio passa de 0 (zero) para 3+.
III- O óxido formado como produto da reação possui os seus átomos ligados entre si por meio de ligações iônicas.
IV- A quantidade de calor liberado, considerando 100% de rendimento na reação, é de aproximadamente 2450 kJ.
V- Nesta reação ocorre a oxidação do ferro.
Das afirmativas feitas, estão corretas apenas
Ver questãoQuestão 82206
ESPCEX
(EsPCEx - 2023)
Durante o curso de formação, um dos experimentos de investigação realizados pelos alunos da EsPCEXx, utilizando o conceito de proteção por meio de ânodo de sacrifício, consiste em polir quatro pregos de ferro, envolver cada um deles com uma fita metálica de diferentes metais e mergulhá-los em uma solução aquosa de ferricianeto de potássio com oxigênio dissolvido. O ferricianeto de potássio é um sal que, em meio aquoso, atua como um indicador de corrosão do ferro, pois adquire coloração azul na presença de ions de ferro. O experimento está representado na imagem ao lado:
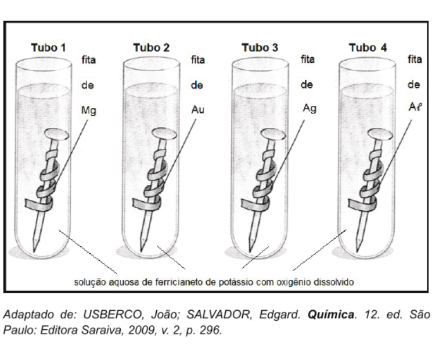
Dados:

Considerando as informações apresentadas, após certo tempo, surgirá coloração azul apenas nos tubos
Ver questão